题目内容
17.小明在做实验时,不小心将镁条掉入到碳酸氢钠溶液中,发现产生大量的气泡和白色不溶物.他非常好奇,进行了如下探究.【提出问题】镁条与碳酸氢钠溶液反应,产生的气体和白色不溶物分别是什么?
【查阅资料】
①MgHCO3能溶于水;Mg(OH)2、MgCO3难溶于水.
②Mg(OH)2、MgCO3受热易分解,分别生成两种氧化物.
③碱石灰的主要成分为氧化钙和氢氧化钠.
【作出猜想】
小明认为白色不溶物的组成存在3种可能,分别为Mg(OH)2;MgCO3;Mg(OH)2和MgCO3.
【进行实验】
(1)探究镁条与碳酸氢钠溶液反应产生什么气体?
| 实验操作 | 实验现象 |
| ①点燃产生的气体 | 气体燃烧,产生蓝色火焰 |
| ②火焰上罩内壁涂有石灰水 的烧杯 | 无现象 |
(2)探究镁条与碳酸氢钠反应后产生的白色不溶物中是否含有MgCO3
| 实验操作及现象 | 实验结论 |
| 将反应后的浊液过滤,洗涤滤渣,向滤渣中加入稀盐酸,有气泡产生,将产生的气体通入到澄清的石灰水中,石灰水变浑浊 | 白色不溶物中一定含有MgCO3 |
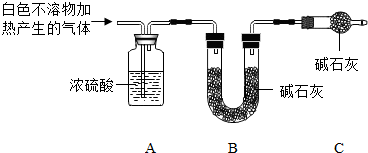
①C中碱石灰的作用是防止空气中的水和二氧化碳进入装置B中.
②若白色不溶物为22.6g,实验前后装置A增重1.8g,装置B增重8.8g,则该白色不溶物的组成及质量比为Mg (OH)2 与MgCO3的质量比为29:84;或MgCO3与Mg (OH)2的质量比为84:29.
分析 【做出猜想】根据题干中提供的信息来分析;
【进行试验】(1)根据实验现象以及质量守定律来分析;
(2)根据碳酸盐的检验方法来分析;
(3)C中的碱石灰是与空气直接接触;根据B中碱石灰质量的增加量就是生成的二氧化碳的质量,根据二氧化碳的质量计算出碳酸镁的质量,剩余的就是氢氧化镁的质量.
解答 解:【作出猜想】由题干信息可知,Mg(OH)2、MgCO3难溶于水的白色固体,则可能是氢氧化镁、碳酸镁或氢氧化镁和碳酸镁的混合物;故填:Mg(OH)2;MgCO3;Mg(OH)2和 MgCO3
【进行实验】
(1)气体安静燃烧、产生淡蓝色火焰,说明该气体具有可燃性,再根据质量守恒定律反应前后元素种类不变,该气体可能是氢气或一氧化碳,如果测定是一氧化碳时,燃烧后需要用到澄清石灰水,所以该气体是氢气;故填:镁条和碳酸氢钠溶液反应产生的气体为氢气.
(2)碳酸镁与稀盐酸反应生成二氧化碳气体,二氧化碳能使澄清的石灰水变浑浊;故填:将反应后的浊液过滤,洗涤滤渣,向滤渣中加入稀盐酸,有气泡产生,将产生的气体通入到澄清的石灰水中,石灰水变浑浊;
(3)①C中的碱石灰可以防止空气中的水和二氧化碳进入装置B中.故填:防止空气中的水和二氧化碳进入装置B中;
②Mg(OH)2和MgCO3,质量比为29:84
【实际应用定量分析】B中碱石灰质量的增加量就是生成的二氧化碳的质量,所以生成二氧化碳的质量为8.8g,设生成8.8g二氧化碳,需要碳酸镁的质量为X则:
MgCO3+2HCl═MgCl2+H2O+CO2↑
84 44
X 8.8g
根据:$\frac{84}{44}=\frac{X}{8.8g}$
X=16.8g,所以含有氢氧化镁质量为:22.6g-16.8g=5.8g;
因此Mg (OH)2 与MgCO3的质量比为5.8g:16.8g=29:84;或MgCO3与Mg (OH)2的质量比为84:29.
故答案为:Mg (OH)2 与MgCO3的质量比为29:84;或MgCO3与Mg (OH)2的质量比为84:29.
点评 本题难度较大,考查全面,从定性和定量两个方面测定物质的种类,关键在于知道碳酸根离子与酸反应能产生二氧化碳.

 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案(1)小张同学先取该无色溶液少许,滴入紫色石蕊试液,石蕊试液变红,此时可得出的结论是该溶液呈酸性.
(2)小王同学发现尽管试剂瓶标签已模糊,但依稀可见SO4字样.于是,他设计了甲、乙两个方案,并分别取样品实验、记录相关现象.
方案甲:样品$\stackrel{加入足量Ba(NO_{3})_{2}溶液}{→}$产生白色沉淀$\stackrel{加入足量稀HNO_{3}}{→}$沉淀不溶解
方案乙:样品$\stackrel{加入足量稀HCl}{→}$无明显现象$\stackrel{加入足量BaCl_{2}溶液}{→}$产生白色沉淀
上述方案中,能确定该无色溶液中含有硫酸根的方案是方案甲、方案乙;
方案乙中,加入足量稀HCl的作用是排除碳酸根离子和银离子的干扰.
(3)同学们发现标签上还有20.0%的字样,老师告诉他们,这瓶试剂是硫酸、硫酸钠、硫酸镁溶液中的一种.同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
| 物质 | H2SO4 | Na2SO4 | MgSO4 |
| 溶解度/g | 与水任意比互溶 | 19.0 | 39.0 |
| A. | 氮气 | B. | 氦气 | C. | 二氧化碳 | D. | 氨气 |
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | NaCl溶液 | Na2CO3 | 加人适量的硝酸钡溶液至不再产生沉淀,过滤 |
| B | CuO粉末 | C | 加人过量的稀盐酸充分反应 |
| C | KCl晶体 | MgO | 溶解、过滤、蒸发 |
| D | CO2 | CO | 在O2中点燃 |
| A. | A | B. | B | C. | C | D. | D |
| 选项 | 事 实 | 解 释 |
| A | 氧化汞受热会得到氧气和汞 | 分子在化学变化中可以再分 |
| B | 盐酸、稀硫酸都能使紫色石蕊试液变红 | 它们所含的阳离子全部都是H+ |
| C | 将墨汁滴入一杯清水中,清水很快变黑 | 分子在不断运动 |
| D | 25m3的氧气可以装入0.024m3的钢瓶中 | 氧分子的体积变小 |
| A. | A | B. | B | C. | C | D. | D |
| A. | Z、Y、X | B. | Y、X、Z | C. | X、Y、Z | D. | Y、Z、X |
| 选项 | 溶液 | 杂质 | 试剂 |
| A | NaNO3溶液 | Na2CO3溶液 | 过量Ba (NO3)2溶液 |
| B | CaCl2溶液 | 稀盐酸 | 足量CaCO3固体 |
| C | 氢气 | 氯化氢 | 先通过过量NaOH溶液,再通过过量浓硫酸 |
| D | Fe2(SO4)3溶液 | Na2SO4溶液 | 适量NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
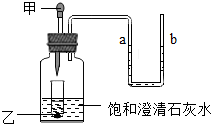 如图,小试管中盛放着固体乙(足量),滴管中有液体甲,广口瓶中有少量饱和的澄清石灰水(试管底部浸没在澄清石灰水中).当把甲溶液滴加到乙中,过一会儿可看到石灰水变浑浊了,U形管中的a液面降低、b液面升高了.请你根据以上现象分析,下列说法不正确的是( )
如图,小试管中盛放着固体乙(足量),滴管中有液体甲,广口瓶中有少量饱和的澄清石灰水(试管底部浸没在澄清石灰水中).当把甲溶液滴加到乙中,过一会儿可看到石灰水变浑浊了,U形管中的a液面降低、b液面升高了.请你根据以上现象分析,下列说法不正确的是( )| A. | 甲、乙可能分别是稀硫酸和碳酸钠 | |
| B. | 甲、乙有可能分别是水和硝酸铵 | |
| C. | 甲、乙可能分别是氧化钙和水 | |
| D. | 石灰水变浑浊,不可能是发生了物理变化 |
