题目内容
5.下表列出了除去物质中所含少量杂质的方法,其中正确的是( )| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | NaCl溶液 | Na2CO3 | 加人适量的硝酸钡溶液至不再产生沉淀,过滤 |
| B | CuO粉末 | C | 加人过量的稀盐酸充分反应 |
| C | KCl晶体 | MgO | 溶解、过滤、蒸发 |
| D | CO2 | CO | 在O2中点燃 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、Na2CO3能与适量的硝酸钡溶液反应生成碳酸钡沉淀和硝酸钠,能除去杂质但引入了新的杂质硝酸钠,不符合除杂原则,故选项所采取的方法错误.
B、CuO粉末能与稀盐酸反应生成氯化铜和水,铜不与稀盐酸反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、KCl晶体易溶于水,MgO难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法正确.
D、除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为除去气体中的气体杂质不能使用气体,否则会引入新的气体杂质,故选项所采取的方法错误.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
17.下列各组物质,前者属于混合物,后者属于化合物的是( )
| A. | 净化后的自来水 铝合金 | B. | 氨气 煤 | ||
| C. | 冰水混合物 液氧 | D. | 石灰水 二氧化碳 |
13.有三瓶失去标签的无色溶液,只知道它们分别是稀盐酸、澄清石灰水和氯化钠溶液中的各一种.下列四种试剂中,能将上述三种无色溶液一次鉴别出来的是( )
| A. | MgCl2溶液 | B. | KNO3溶液 | C. | Na2CO3溶液 | D. | NaOH溶液 |
20.下列实验现象描述正确的是( )
| A. | 木炭在空气中燃烧,生成二氧化碳 | |
| B. | 红磷在空气中燃烧,产生浓厚的白烟 | |
| C. | 硫在空气中燃烧,产生明亮的蓝紫色火焰 | |
| D. | 细铁丝在空气中燃烧,火星四射,生成黑色固体 |
17.小明在做实验时,不小心将镁条掉入到碳酸氢钠溶液中,发现产生大量的气泡和白色不溶物.他非常好奇,进行了如下探究.
【提出问题】镁条与碳酸氢钠溶液反应,产生的气体和白色不溶物分别是什么?
【查阅资料】
①MgHCO3能溶于水;Mg(OH)2、MgCO3难溶于水.
②Mg(OH)2、MgCO3受热易分解,分别生成两种氧化物.
③碱石灰的主要成分为氧化钙和氢氧化钠.
【作出猜想】
小明认为白色不溶物的组成存在3种可能,分别为Mg(OH)2;MgCO3;Mg(OH)2和MgCO3.
【进行实验】
(1)探究镁条与碳酸氢钠溶液反应产生什么气体?
通过上述实验得到的结论是镁条和碳酸氢钠溶液反应产生的气体为氢气.
(2)探究镁条与碳酸氢钠反应后产生的白色不溶物中是否含有MgCO3
(3)定量测定白色不溶物的组成在老师的帮助下,小明设计了如下装置进行实验.
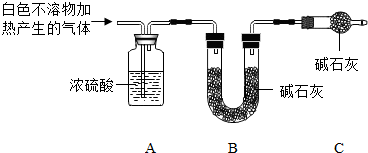
①C中碱石灰的作用是防止空气中的水和二氧化碳进入装置B中.
②若白色不溶物为22.6g,实验前后装置A增重1.8g,装置B增重8.8g,则该白色不溶物的组成及质量比为Mg (OH)2 与MgCO3的质量比为29:84;或MgCO3与Mg (OH)2的质量比为84:29.
【提出问题】镁条与碳酸氢钠溶液反应,产生的气体和白色不溶物分别是什么?
【查阅资料】
①MgHCO3能溶于水;Mg(OH)2、MgCO3难溶于水.
②Mg(OH)2、MgCO3受热易分解,分别生成两种氧化物.
③碱石灰的主要成分为氧化钙和氢氧化钠.
【作出猜想】
小明认为白色不溶物的组成存在3种可能,分别为Mg(OH)2;MgCO3;Mg(OH)2和MgCO3.
【进行实验】
(1)探究镁条与碳酸氢钠溶液反应产生什么气体?
| 实验操作 | 实验现象 |
| ①点燃产生的气体 | 气体燃烧,产生蓝色火焰 |
| ②火焰上罩内壁涂有石灰水 的烧杯 | 无现象 |
(2)探究镁条与碳酸氢钠反应后产生的白色不溶物中是否含有MgCO3
| 实验操作及现象 | 实验结论 |
| 将反应后的浊液过滤,洗涤滤渣,向滤渣中加入稀盐酸,有气泡产生,将产生的气体通入到澄清的石灰水中,石灰水变浑浊 | 白色不溶物中一定含有MgCO3 |

①C中碱石灰的作用是防止空气中的水和二氧化碳进入装置B中.
②若白色不溶物为22.6g,实验前后装置A增重1.8g,装置B增重8.8g,则该白色不溶物的组成及质量比为Mg (OH)2 与MgCO3的质量比为29:84;或MgCO3与Mg (OH)2的质量比为84:29.
14.酸溶液中都含有H+,因此不同的酸表现出一些共同的性质.下列关于稀硫酸性质的描述不属于酸的共同性质的是( )
| A. | 能使紫色石蕊溶液变红色 | B. | 能与锌反应生成氢气 | ||
| C. | 能与碳酸钠溶液反应生成二氧化碳 | D. | 能与氯化钡溶液反应生成沉淀 |
15.下列物质中,属于混合物的是( )
| A. | 碘酒 | B. | 碳酸氢钠 | C. | 氢氧化钾 | D. | 过氧化氢 |
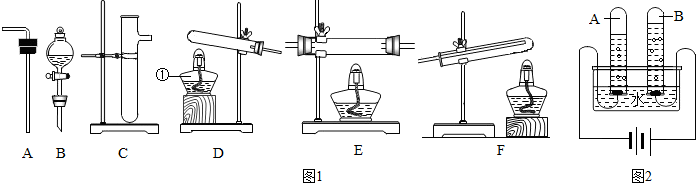
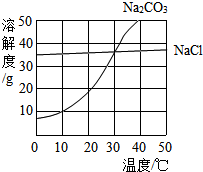 如图为氯化钠、碳酸钠在水中的溶解度曲线,根据图示回答问题.
如图为氯化钠、碳酸钠在水中的溶解度曲线,根据图示回答问题.