题目内容
7.实验室有一瓶无色溶液,标签已模糊,为探究该溶液中的溶质究竟是什么物质,某兴趣小组的同学进行了一系列实验:(1)小张同学先取该无色溶液少许,滴入紫色石蕊试液,石蕊试液变红,此时可得出的结论是该溶液呈酸性.
(2)小王同学发现尽管试剂瓶标签已模糊,但依稀可见SO4字样.于是,他设计了甲、乙两个方案,并分别取样品实验、记录相关现象.
方案甲:样品$\stackrel{加入足量Ba(NO_{3})_{2}溶液}{→}$产生白色沉淀$\stackrel{加入足量稀HNO_{3}}{→}$沉淀不溶解
方案乙:样品$\stackrel{加入足量稀HCl}{→}$无明显现象$\stackrel{加入足量BaCl_{2}溶液}{→}$产生白色沉淀
上述方案中,能确定该无色溶液中含有硫酸根的方案是方案甲、方案乙;
方案乙中,加入足量稀HCl的作用是排除碳酸根离子和银离子的干扰.
(3)同学们发现标签上还有20.0%的字样,老师告诉他们,这瓶试剂是硫酸、硫酸钠、硫酸镁溶液中的一种.同学通过查阅资料得知,常温下这三种物质的溶解度如下表:
| 物质 | H2SO4 | Na2SO4 | MgSO4 |
| 溶解度/g | 与水任意比互溶 | 19.0 | 39.0 |
分析 (1)根据酸性溶液能使紫色石蕊试液变红进行解答;
(2)根据硫酸根离子和硝酸钡反应生成硫酸钡沉淀,且硫酸钡白色沉淀不溶于稀硝酸,样品中加入足量稀盐酸没有明显的现象,说明样品中不含有碳酸根离子和银离子,再加入氯化钡溶液产生白色沉淀,说明生成了硫酸钡白色沉淀进行解答;
(3)根据溶解度计算,在该温度下,饱和溶液中的溶质的质量分数进行解答.
解答 解:(1)酸性溶液能使紫色石蕊试液变红,所以取该无色溶液少许,滴入紫色石蕊试液,石蕊试液变红,此时可得出的结论是该溶液呈酸性;故填:该溶液呈酸性;
(2)硫酸根离子和硝酸钡反应生成硫酸钡沉淀,且硫酸钡白色沉淀不溶于稀硝酸,所以方案甲可行;样品中加入足量稀盐酸没有明显的现象,说明样品中不含有碳酸根离子和银离子,再加入氯化钡溶液产生白色沉淀,说明生成了硫酸钡白色沉淀,所以方案乙也可行;故填:方案甲、方案乙;排除碳酸根离子和银离子的干扰;
(3)根据硫酸钠的溶解度,在该温度下,硫酸钠饱和溶液的溶质的质量分数为:$\frac{19.0g}{100g+19.0g}$×100%≈17%,即最大质量分数不会超过17%,而图中信息为20%,则一定不是硫酸钠溶液.故填:常温下硫酸钠溶液的最大质量分数是17%,不能配置出20%的溶液.
点评 掌握常见的离子的检验方法是正确解答本题的关键.加强对化学基础知识的掌握,以便做出正确判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.硅酸盐中的硅酸钠Na2SiO3具有软化血管的作用,其中硅元素的化合价是( )
| A. | +2 | B. | +4 | C. | +1 | D. | +2 |
20.过氧化苯甲酰是面粉增白剂,可以改变面粉外观,却能破坏面粉中叶酸等微量营养素,增加人的肝脏负担,过氧化苯甲酰的分子式为C14H10O4.下列关于过氧化苯甲酰的说法错误的是( )
| A. | 过氧化苯甲酰中含有14个碳原子、10个氢原子和4个氧原子 | |
| B. | 过氧化苯甲酰属于有机物 | |
| C. | 过氧化苯甲酰由三种元素组成 | |
| D. | 过氧化苯甲酰中碳元素的质量分数为69.4% |
17.下列各组物质,前者属于混合物,后者属于化合物的是( )
| A. | 净化后的自来水 铝合金 | B. | 氨气 煤 | ||
| C. | 冰水混合物 液氧 | D. | 石灰水 二氧化碳 |
2.下列过程中,有一个去污原理与其他三个不同的是( )
| A. | 用洗涤剂洗去餐具上的油脂 | |
| B. | 用酒精除去附着在试管内壁的碘 | |
| C. | 用汽油除去衣服上的油污 | |
| D. | 用热水洗去附着在烧杯底部的硝酸钾 |
17.小明在做实验时,不小心将镁条掉入到碳酸氢钠溶液中,发现产生大量的气泡和白色不溶物.他非常好奇,进行了如下探究.
【提出问题】镁条与碳酸氢钠溶液反应,产生的气体和白色不溶物分别是什么?
【查阅资料】
①MgHCO3能溶于水;Mg(OH)2、MgCO3难溶于水.
②Mg(OH)2、MgCO3受热易分解,分别生成两种氧化物.
③碱石灰的主要成分为氧化钙和氢氧化钠.
【作出猜想】
小明认为白色不溶物的组成存在3种可能,分别为Mg(OH)2;MgCO3;Mg(OH)2和MgCO3.
【进行实验】
(1)探究镁条与碳酸氢钠溶液反应产生什么气体?
通过上述实验得到的结论是镁条和碳酸氢钠溶液反应产生的气体为氢气.
(2)探究镁条与碳酸氢钠反应后产生的白色不溶物中是否含有MgCO3
(3)定量测定白色不溶物的组成在老师的帮助下,小明设计了如下装置进行实验.
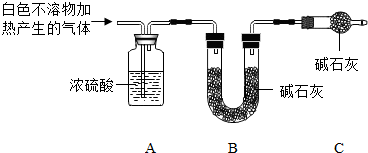
①C中碱石灰的作用是防止空气中的水和二氧化碳进入装置B中.
②若白色不溶物为22.6g,实验前后装置A增重1.8g,装置B增重8.8g,则该白色不溶物的组成及质量比为Mg (OH)2 与MgCO3的质量比为29:84;或MgCO3与Mg (OH)2的质量比为84:29.
【提出问题】镁条与碳酸氢钠溶液反应,产生的气体和白色不溶物分别是什么?
【查阅资料】
①MgHCO3能溶于水;Mg(OH)2、MgCO3难溶于水.
②Mg(OH)2、MgCO3受热易分解,分别生成两种氧化物.
③碱石灰的主要成分为氧化钙和氢氧化钠.
【作出猜想】
小明认为白色不溶物的组成存在3种可能,分别为Mg(OH)2;MgCO3;Mg(OH)2和MgCO3.
【进行实验】
(1)探究镁条与碳酸氢钠溶液反应产生什么气体?
| 实验操作 | 实验现象 |
| ①点燃产生的气体 | 气体燃烧,产生蓝色火焰 |
| ②火焰上罩内壁涂有石灰水 的烧杯 | 无现象 |
(2)探究镁条与碳酸氢钠反应后产生的白色不溶物中是否含有MgCO3
| 实验操作及现象 | 实验结论 |
| 将反应后的浊液过滤,洗涤滤渣,向滤渣中加入稀盐酸,有气泡产生,将产生的气体通入到澄清的石灰水中,石灰水变浑浊 | 白色不溶物中一定含有MgCO3 |

①C中碱石灰的作用是防止空气中的水和二氧化碳进入装置B中.
②若白色不溶物为22.6g,实验前后装置A增重1.8g,装置B增重8.8g,则该白色不溶物的组成及质量比为Mg (OH)2 与MgCO3的质量比为29:84;或MgCO3与Mg (OH)2的质量比为84:29.