题目内容
12.高纯度的氧化铜可用作颜料、有机合成催化剂等,以下是工业用粗铜粉氧化法获取高纯度氧化铜的流程图.
(1)洗涤固体B所用的试剂为稀硫酸.
(2)②中反应的化学方程式为Fe+CuSO4═FeSO4+Cu,Fe+H2SO4═FeSO4+H2↑.
分析 (1)根据固体B中含有过量的铁分析回答;
(2)根据滤液A中含有硫酸和硫酸铜分析加入过量的铁发生的反应.
解答 解:(1)由变化的过程可知,固体B中含有铁粉,可以加入稀硫酸除去铁粉;
(2)由于液A中含有硫酸和硫酸铜,加入铁反应的反应有:Fe+CuSO4═FeSO4+Cu,Fe+H2SO4═FeSO4+H2↑.
故答为:(1)稀硫酸(或硫酸铜溶液) (2)Fe+CuSO4═FeSO4+Cu,Fe+H2SO4═FeSO4+H2↑.
点评 本题以粗铜粉氧化法生产高纯度CuO的流程图来考查学生物质的转化及基本的实验操作,明确每步转化后物质的成分及转化中的反应是解答的关键.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
2.下列过程中,有一个去污原理与其他三个不同的是( )
| A. | 用洗涤剂洗去餐具上的油脂 | |
| B. | 用酒精除去附着在试管内壁的碘 | |
| C. | 用汽油除去衣服上的油污 | |
| D. | 用热水洗去附着在烧杯底部的硝酸钾 |
20.下列实验现象描述正确的是( )
| A. | 木炭在空气中燃烧,生成二氧化碳 | |
| B. | 红磷在空气中燃烧,产生浓厚的白烟 | |
| C. | 硫在空气中燃烧,产生明亮的蓝紫色火焰 | |
| D. | 细铁丝在空气中燃烧,火星四射,生成黑色固体 |
7.在实验室中,下列做法正确的是 ( )
| A. | 对某些药品,为了更明确性质,可把鼻孔凑到容器口去闻一闻气味或尝一下药品的味道 | |
| B. | 打碎的玻璃仪器,要用一只专门的废物箱盛装,集满一箱后,送到废品收购站 | |
| C. | 用双氧水制氧气后的废液需要回收,然后集中静置、过滤、晾干,获得的二氧化锰固体可供下次实验使用 | |
| D. | 实验室剩余的药品不要随意丢弃,可拿回家继续做实验 | |
| E. | 做实验时,为了取得更好的实验效果,应尽可能多的添加药品以便观察 | |
| F. | 做完实验离开实验室前,应关闭水管和电源,将试验台物品整理干净. |
17.小明在做实验时,不小心将镁条掉入到碳酸氢钠溶液中,发现产生大量的气泡和白色不溶物.他非常好奇,进行了如下探究.
【提出问题】镁条与碳酸氢钠溶液反应,产生的气体和白色不溶物分别是什么?
【查阅资料】
①MgHCO3能溶于水;Mg(OH)2、MgCO3难溶于水.
②Mg(OH)2、MgCO3受热易分解,分别生成两种氧化物.
③碱石灰的主要成分为氧化钙和氢氧化钠.
【作出猜想】
小明认为白色不溶物的组成存在3种可能,分别为Mg(OH)2;MgCO3;Mg(OH)2和MgCO3.
【进行实验】
(1)探究镁条与碳酸氢钠溶液反应产生什么气体?
通过上述实验得到的结论是镁条和碳酸氢钠溶液反应产生的气体为氢气.
(2)探究镁条与碳酸氢钠反应后产生的白色不溶物中是否含有MgCO3
(3)定量测定白色不溶物的组成在老师的帮助下,小明设计了如下装置进行实验.
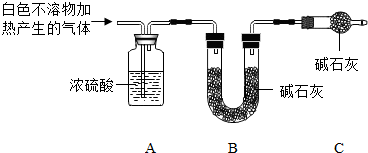
①C中碱石灰的作用是防止空气中的水和二氧化碳进入装置B中.
②若白色不溶物为22.6g,实验前后装置A增重1.8g,装置B增重8.8g,则该白色不溶物的组成及质量比为Mg (OH)2 与MgCO3的质量比为29:84;或MgCO3与Mg (OH)2的质量比为84:29.
【提出问题】镁条与碳酸氢钠溶液反应,产生的气体和白色不溶物分别是什么?
【查阅资料】
①MgHCO3能溶于水;Mg(OH)2、MgCO3难溶于水.
②Mg(OH)2、MgCO3受热易分解,分别生成两种氧化物.
③碱石灰的主要成分为氧化钙和氢氧化钠.
【作出猜想】
小明认为白色不溶物的组成存在3种可能,分别为Mg(OH)2;MgCO3;Mg(OH)2和MgCO3.
【进行实验】
(1)探究镁条与碳酸氢钠溶液反应产生什么气体?
| 实验操作 | 实验现象 |
| ①点燃产生的气体 | 气体燃烧,产生蓝色火焰 |
| ②火焰上罩内壁涂有石灰水 的烧杯 | 无现象 |
(2)探究镁条与碳酸氢钠反应后产生的白色不溶物中是否含有MgCO3
| 实验操作及现象 | 实验结论 |
| 将反应后的浊液过滤,洗涤滤渣,向滤渣中加入稀盐酸,有气泡产生,将产生的气体通入到澄清的石灰水中,石灰水变浑浊 | 白色不溶物中一定含有MgCO3 |

①C中碱石灰的作用是防止空气中的水和二氧化碳进入装置B中.
②若白色不溶物为22.6g,实验前后装置A增重1.8g,装置B增重8.8g,则该白色不溶物的组成及质量比为Mg (OH)2 与MgCO3的质量比为29:84;或MgCO3与Mg (OH)2的质量比为84:29.
4.襄阳各地盛产松花蛋,又称皮蛋、变蛋,其中一种加工工艺的主要原料配方为:鸭蛋10Kg,水10Kg,生石灰1.2Kg,纯碱0.53Kg,食盐0.35Kg.加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍.请回答下列问题:
(1)生石灰加入沸水中,水能持续保持沸腾,其原因是生石灰与水反应过程中放出大量的热.
(2)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色
(3)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaOH、NaCl
②可能还含有其它溶质:甲同学推断只有Ca(OH)2,乙同学推断只有Na2CO3,丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示).
【实验探究】
【探究结论】甲同学的推断是正确的.
(1)生石灰加入沸水中,水能持续保持沸腾,其原因是生石灰与水反应过程中放出大量的热.
(2)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色
(3)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaOH、NaCl
②可能还含有其它溶质:甲同学推断只有Ca(OH)2,乙同学推断只有Na2CO3,丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示).
【实验探究】
| 实验步骤 | 实验现象 |
| 取少量上层料液,滴加稀盐酸 | 无明显现象 |
| 另取少量上层料液,滴加碳酸钠溶液 | 产生白色沉淀 |
1.下列各组物质中,均属纯净物的是( )
| A. | 合成纤维 玻璃 | B. | 可燃冰 水银 | C. | 冰水 干冰 | D. | 医用酒精 碘盐 |
