题目内容
2.某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂.该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体.【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠 猜想b:碳酸氢钠
小周同学认为猜想b不成立,理由是反应物中不含有氢元素,不能生成碳酸氢钠.
【实验】取少量生成的白色固体于试管中,加入稀盐酸或稀硫酸,产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊.
稀盐酸(稀HCl)
【结论】猜想a成立.
请写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
【继续探究】过氧化钠能否与水反应?生成物是什么?
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量过氧化钠粉末于试管中,加入蒸馏水,再用带火星的木条伸入试管中 | 产生气泡 带火星的木条复燃 | 过氧化钠能与水反应生成氧气 |
| ②向上述反应后的试管中滴加酚酞试液 | 酚酞试液变红色 | 所得溶液呈碱性,推断过氧化钠与水反应生成NaOH (填化学式) |
分析 【猜想】化学反应遵循质量守恒定律,即反应前后元素种类不变,原子种类和总个数不变;
【实验】碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,能和稀硫酸反应生成硫酸钠、水和二氧化碳;
二氧化碳能和氢氧化钙反应生成白色沉淀碳酸钙和水,因此二氧化碳能使澄清石灰水变浑浊;
碳酸钠能和二氧化碳反应生成碳酸钠和氧气;
【继续探究】氧气能使带火星的木条复燃;
显碱性的溶液能使酚酞试液变红色;
【交流与反思】通常情况下能和空气中的成分发生化学反应的物质应该密封保存.
解答 解:【猜想】
因为反应物中不含有氢元素,根据质量守恒定律可知,过氧化钠和二氧化碳反应不能生成碳酸氢钠,因此猜想b不成立.
故填:反应物中不含有氢元素,不能生成碳酸氢钠.
【实验】
取少量生成的白色固体于试管中,加入稀盐酸或稀硫酸,产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊,说明反应生成了二氧化碳气体;
过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2.
故填:稀盐酸或稀硫酸;2Na2O2+2CO2=2Na2CO3+O2.
【继续探究】
①取少量过氧化钠粉末于试管中,加入蒸馏水,再用带火星的木条伸入试管中,观察到产生气泡,带火星的木条复燃,说明反应生成了氧气,进一步说明过氧化钠和水反应生成了氧气;
②向上述反应后的试管中滴加酚酞试液,酚酞试液变红色,说明生成了显碱性的物质,根据质量守恒定律可知,过氧化钠和水反应能够生成氢氧化钠,填表如下所示:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量过氧化钠粉末于试管中,加入蒸馏水,再用带火星的木条伸入试管中 | 产生气泡 带火星的木条复燃 | 过氧化钠能与水反应生成氧气 |
| ②向上述反应后的试管中滴加酚酞试液 | 酚酞试液变红色 | 所得溶液呈碱性,推断过氧化钠与水反应生成 NaOH |
由于过氧化钠常温下能与二氧化碳和水反应,所以保存过氧化钠一定要与二氧化碳和水隔绝,因此应该密封保存.
故填:密封保存.
点评 过氧化钠和水中含有钠元素、氧元素和氢元素,反应时能够产生能使酚酞试液变红色的显碱性的物质,只能够生成氢氧化钠这种显碱性的物质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.请根据题目要求填空.
【实验】将一定量的稀盐酸加入到盛有饱和氢氧化钙溶液的烧杯中.
【提出问题】反应后溶液中溶质是什么?
【假设猜想】甲组同学的猜想如下,请在横线上写出猜想四.
猜想一:只有CaCl2
猜想二:有CaCl2和HCl
猜想三:有CaCl2、HCl和Ca(OH)2
猜想四:有CaCl2和Ca(OH)2.
【质疑】乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.
不合理的猜想是:猜想三,理由是盐酸和氢氧化钙不能共存.
【实验操作】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有Ca(OH)2.
(2)为了探究究竟是哪种猜想成立,丁组同学取适量反应后的溶液进行实验,选用了老师提供的pH试纸和一些溶液,依次进行一下两个实验,完成下列实验报告.
限选试剂:Ba(OH)2溶液、NaCl溶液、AgNO3溶液、Na2CO3溶液.
【实验】将一定量的稀盐酸加入到盛有饱和氢氧化钙溶液的烧杯中.
【提出问题】反应后溶液中溶质是什么?
【假设猜想】甲组同学的猜想如下,请在横线上写出猜想四.
猜想一:只有CaCl2
猜想二:有CaCl2和HCl
猜想三:有CaCl2、HCl和Ca(OH)2
猜想四:有CaCl2和Ca(OH)2.
【质疑】乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.
不合理的猜想是:猜想三,理由是盐酸和氢氧化钙不能共存.
【实验操作】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有Ca(OH)2.
(2)为了探究究竟是哪种猜想成立,丁组同学取适量反应后的溶液进行实验,选用了老师提供的pH试纸和一些溶液,依次进行一下两个实验,完成下列实验报告.
限选试剂:Ba(OH)2溶液、NaCl溶液、AgNO3溶液、Na2CO3溶液.
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1:用洁净干燥的玻璃棒蘸取溶液,粘在pH试纸上,与标准比色卡对照 | 试纸变色,溶液pH<7 | 溶液中有HCl |
| 步骤2:取少量反应后溶液于试管中,滴加碳酸钠溶液振荡 | 先产生气泡,后产生沉淀 | 溶液中有CaCl2 |
7.下列物质不能与氢氧化钠反应的是( )
| A. | 紫色石蕊试液 | B. | CuO | C. | CO2 | D. | H2SO4 |
11.人体内含量最高的金属元素( )
| A. | 氢 | B. | 钠 | C. | 钙 | D. | 铁 |
 ”和“
”和“ ”分别表示氮原子和氧原子,如图2是氮气与氧气在放电条件下发生反应的微观模拟图,请回答下列问题:
”分别表示氮原子和氧原子,如图2是氮气与氧气在放电条件下发生反应的微观模拟图,请回答下列问题: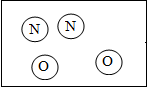 ,你的理论依据是反应前后原子种类、个数不变.
,你的理论依据是反应前后原子种类、个数不变.