题目内容
14.水是地球表面覆盖最多的物质,也是生命活动不可缺少的物质.
(1)下列关于水的说法中,不正确的由:②④(填序号).
①水是由氢元素和氧元素组成的化合物;②清澈、透明的泉水是纯净物;③合理施用农药、化肥.以减少水体污染;④将活性炭放入硬水中可使其软化;⑤洗菜、洗衣后的水用来浇花、冲洗厕所.
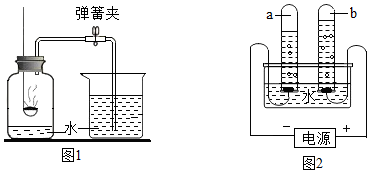
(2)电解水实验揭示了水的组成.如图1实验中得到氧气的试管是2(填“1”或“2”).写出实验室电解水反应的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
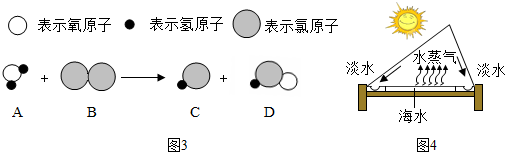
(3)城镇自来水厂生产流程可用如图2表示:
除去水中固态杂质的设备是:过滤池;投药的作用是消毒杀菌.如图3表示自来水消毒过程中发生的一个反应的微观过程:
请写出上述反应的化学方程式H2O+Cl2=HCl+HClO.
(4)海水淡化可缓解淡水资源匮乏的问题.如图4为太阳能海水淡化装置示意图.水变成水蒸气的过程中,发生变化的是C(填字母序号).
A、分子质量 B、分子种类 C、分子间隔
上述所获取的水为软水(填“硬水”或“软水”).
分析 (1)根据水的组成、性质、用途分析;
(2)根据化学式书写原则、过滤的适用范围、装置及仪器分析
(3)根据硬水软水的区分方法软化方法分析
(4)根据化学反应的微观示意图写出化学式、根据化学式确定出化合价.
解答 解:(1)水是由氢元素和氧元素组成的化合物;清澈、透明的泉水里面含有多种矿物质,属于混合物;合理施用农药、化肥可以减少水体污染;活性炭不能使硬水软化;洗菜、洗衣后的水用来浇花、冲洗厕所可做到节约用水.故选:②④;
(2)电解水实验中与电源负极相连的玻璃管中产生的是氢气,正极相连的玻璃管中产生的是氧气,水在通电的条件下生成氢气和氧气,其化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;故填:2; 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(3)在自来水净化过程中,除去水中固态杂质的设备是过滤池;投药的作用是消毒杀菌.图3表示自来水消毒过程中发生的一个反应的微观过程,其反应的化学方程式为H2O+Cl2=HCl+HClO.故填:过滤池;消毒杀菌;H2O+Cl2=HCl+HClO;
(4)水变成水蒸气的过程中,发生变化的是分子间隔,经过以上过程净化后得到的水是软水.故填:分子间隔;软水;
点评 本题考查电解水实验、过滤、硬水软水等有关水的知识点,属基础知识考查.

练习册系列答案
相关题目
2.某实验小组的同学为了测定实验室中高锰酸钾样品的质量分数,取7g该样品,依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
试计算:
(1)加热t3时间后高锰酸钾是否已经完全反应?是(填“是”或“否”);高锰酸钾中锰、氧元素的质量比为55:64.
(2)求完全反应后产生氧气的质量.
(3)求该样品中高锰酸钾的质量分数.(精确到0.1%)
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量/g | 6.88 | 6.55 | 6.36 | 6.36 |
(1)加热t3时间后高锰酸钾是否已经完全反应?是(填“是”或“否”);高锰酸钾中锰、氧元素的质量比为55:64.
(2)求完全反应后产生氧气的质量.
(3)求该样品中高锰酸钾的质量分数.(精确到0.1%)
3.下列有关化学实验的说法中不正确的是( )
| A. | 用高锰酸钾制02时,反应试管的管口应略向上倾斜 | |
| B. | 做铁在02中燃烧实验时,集气瓶应先放少量水或细沙 | |
| C. | 铁、锌、碘元素都属于微量元素 | |
| D. | 用金属和酸制H2时,可采用与制C02相同的发生装置 |
4. 研究和控制化学反应条件有重要意义.同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
研究和控制化学反应条件有重要意义.同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
(1)取用二氧化锰的仪器是B(填编号).

(2)写出上述反应的文字表达式:过氧化$\stackrel{二氧化锰}{→}$氢水+氧气.
(3)实验3中,加入的二氧化锰质量应为5g.
(4)相同条件下,实验3产生氧气的速率最快,说明双氧水的浓度越大,反应速率越快.
【注意:若答对第(5)小题奖励4分,全卷总分不超过60分】
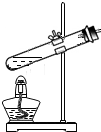
(5)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图中装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,请设计改进实验证明加热双氧水也可产生氧气:用排水法收集氧气并检验.
 研究和控制化学反应条件有重要意义.同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
研究和控制化学反应条件有重要意义.同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间. | 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |

(2)写出上述反应的文字表达式:过氧化$\stackrel{二氧化锰}{→}$氢水+氧气.
(3)实验3中,加入的二氧化锰质量应为5g.
(4)相同条件下,实验3产生氧气的速率最快,说明双氧水的浓度越大,反应速率越快.
【注意:若答对第(5)小题奖励4分,全卷总分不超过60分】
(5)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图中装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,请设计改进实验证明加热双氧水也可产生氧气:用排水法收集氧气并检验.