题目内容
10.在金属活动性顺序中,金属的位置越靠前,它的活动性就越强,在化学反应中越容易失去电子.(I)Ca、Mg、K三种金属在化学反应中失去电子的能力由强到弱的顺序是K>Ca>Mg.
(2)Ca、Mg、K三种金属的原子结构示意图如图
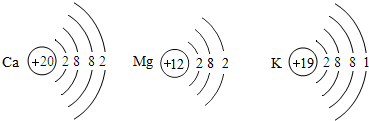
请根据这三种金属的原子结构示意图,结合已学过的有关原子结构的知识推测:金属单质失去电子能力的强弱主要与哪些因素有关?最外层电子数、电子层数有关.
(3)能证明Cu的金属活动性比Ag强的方法是Cu+2AgN03=Cu(N03)2+2Ag(用化学方程式表示).
(4)非金属单质也具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来.例如,在溶液中可发生以下反应:C12+2NaBr=2NaCl+Br2,Br2+2KI=2KBr+I2,I2+Na2S=2NaI+S.由此可以判断硫(S)、溴(Br2)、碘(I2)、氯气(Cl2)四种非金属单质的活动性由弱到强的顺序是S<I2<Br2<Cl2.
分析 (1)由在金属活动性顺序表里,金属的位置越靠前,它的活动性就越强,在化学反应中越容易失去电子,可以进行分析判断.
(2)决定元素化学性质的是最外层电子数,原子的电子层数越多,在最外层电子数一定的条件下,就越容易失去电子,据此分析.
(3)前面的金属可以把排在它后面的金属从盐溶液中置换出来,根据这一规律可以判断反应是否发生及金属的活动性强弱.
(4)由信息:活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,分析解答.
解答 解:(1)Ca、Mg、K三种金属活动性强弱顺序为K>Ca>Mg,故根据题目所给信息可知,在化学反应中失去电子的能力由强到弱的顺序是K>Ca>Mg.
(2)决定元素化学性质的是最外层电子数,原子的电子层数越多,在最外层电子数一定的条件下,就越容易失去电子,故金属单质失去电子能力的强弱主要与最外层电子数、电子层数有关.
(3)由于铜的化学性质比银活泼,因此可以选择铜和硝酸银溶液反应来证明铜比银活泼,反应的方程式是:Cu+2AgN03=Cu(N03)2+2Ag;
(4)非金属单质也具有类似的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,由反应Cl2+2NaBr=2NaCl+Br2可得非金属性Cl2>Br2,同理可得I2>S,Br2>I2,故选Cl2>Br2>I2>S.即四种非金属单质的活动性由弱到强的顺序的S<I2<Br2<Cl2.
故答案为:(1)K>Ca>Mg;
(2)最外层电子数; 电子层数;
(3)Cu+2AgN03=Cu(N03)2+2Ag;
(4)S<I2<Br2<Cl2.
点评 本题难度中等,注重了和课本所学知识的联系,做到知识的迁移应用,检验学生活学活用的学习能力.

练习册系列答案
相关题目
20.从物质分类的角度看,冰水混合物属于( )
| A. | 有机物 | B. | 氧化物 | C. | 单质 | D. | 混合物 |
19.近期我国在一些白酒中查出了对人体有害的塑化剂,其主要成分是邻苯二甲酸二酯,它的化学式为(C24H38O4),下列有关说法正确的是( )
| A. | 该物质中碳、氢、氧三种元素的质量比为24:38:4 | |
| B. | 该物质中碳元素的质量分数为73.8% | |
| C. | 该物质的相对分子质量为400 | |
| D. | 39g塑化剂中含3.9g氢元素 |
20.下列各组物质中,按混合物、化合物、单质顺序排列的是( )
| A. | 氧化镁、酒精、水银 | B. | 净化后的空气、二氧化碳、液态氧 | ||
| C. | 食醋、糖水、天然气 | D. | 冰水共存物、食盐水、氮气 |





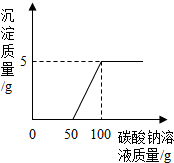 实验室制取二氧化碳后,将废液过滤,得到含有氯化钙和稀盐酸的混合液,20℃
实验室制取二氧化碳后,将废液过滤,得到含有氯化钙和稀盐酸的混合液,20℃