题目内容
18.从化学的视角认识生活中的有关问题.(1)红薯营养丰富,富含淀粉、蛋白质、维生素、锌、铁、钙、硒等.“锌、钙、硒”是指元素(填“单质”、“元素”或“分子”).
(2)维生素在调节人体新陈代谢、预防疾病、维持身体健康方面起到重要作用,缺乏维生素会引起很多疾病,例如缺乏维生素A会引起夜盲症.
(3)洗涤剂能清洗餐具上的油污,这是因为洗涤剂具有乳化功能.
(4)烧开水的铝壶内壁有水垢[主要成分为CaCO3、Mg(OH)2]时,可用厨房调料洗去,除垢时间不宜过长的原因是铝可和多余的醋酸发生化学反应..
分析 (1)根据糖类、蛋白质、脂肪能供给人体能量,水、维生素、无机盐不能为人体供能,;“锌、钙、硒”是指元素进行解答;
(2)根据维生素的作用分析;
(3)根据洗洁精具有乳化作用进行分析;
(4)根据醋酸会与金属氧化物反应反应生成盐和水,醋酸能与活泼金属反应生成氢气进行分析.
解答 解:(1)锌、钙、硒是对所有锌、钙、硒原子的总称,意即该元素,而不是原子,也不是单质.故指的是元素;
(2)缺乏维生素A会引起会引起夜盲症;
(3)洗涤剂有乳化作用,能将大的油滴分散成细小的油滴随水冲走;
(4)铝壶的保护膜是氧化铝,能与醋酸反应反应生成醋酸铝与水,氧化铝反应后醋酸和铝反应生成醋酸铝和氢气,从而对铝壶有所损伤.
故答案为:(1)元素;
(2)夜盲症;
(3)乳化;
(4)铝可和多余的醋酸发生化学反应.
点评 本题难度不大,可依据已有的知识进行.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案
相关题目
6.几年前,一辆载满20t电石的挂车,在浙江滨江区燃起熊熊大火并伴有大量黑烟.事故路面上洒落了五六百米燃着的石头.这辆货车在雨中整整燃烧了一天,消防官兵对大火也束手无措,场面让人震撼.大家对电石的化学性质产生了浓厚的兴趣,请你一起与他们完成下列探究活动.
【查阅资料】电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟.
【猜想与假设】电石与水反应生成的可燃性气体是:氧气、氢气或乙炔(C2H2);电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙.大家做出以上推断的理由是质量守恒定律反应前后元素的种类不变
大家讨论后一致认为该气体不可能是氧气,原因是氧气不能燃烧,白色固体不可能是氧化钙,原因是(用化学方程式表示)CaO+H2O=Ca(OH)2.
【实验探究】
【查阅资料】电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟.
【猜想与假设】电石与水反应生成的可燃性气体是:氧气、氢气或乙炔(C2H2);电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙.大家做出以上推断的理由是质量守恒定律反应前后元素的种类不变
大家讨论后一致认为该气体不可能是氧气,原因是氧气不能燃烧,白色固体不可能是氧化钙,原因是(用化学方程式表示)CaO+H2O=Ca(OH)2.
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃. | 气体燃烧,产生黄色火焰并伴有浓烈黑烟. | 电石与水反应产生的气体是乙炔(C2H2) |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸. | 固体溶解,不产生气泡. | 电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后生成的固体于试管中加水,向上层清液中滴加2~3滴无色酚酞. | 溶液变红 | 电石与水反应产生的固体是氢氧化钙 |
13.体育课上同学们在做引体向上时常用“镁粉”搓手,以起到防滑效果.某种“镁粉”中可能含有Mg、MgO、Mg(OH)2、MgCO3中的一种或两种固体,实验小组对其成分展开了探究.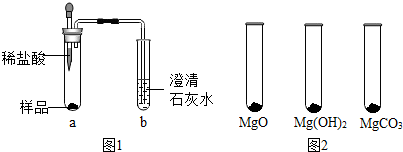
已知:MgO+2HCl═MgCl2+H2O MgCO3+2HCl═MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3.
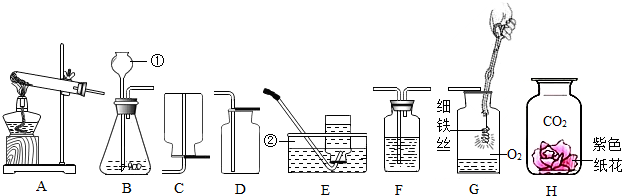
①取少量样品,如图1所示进行实验,观察到a试管中有气泡产生,b试管中产生的现象是澄清石灰水变浑浊,则证明“镁粉”中一定含有MgCO3.
②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭,但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成浓NaOH溶液,目的是除掉二氧化碳.小明按照修改后的实验方案重复上述实验,观察到b试管口,证明“镁粉”中不含Mg.
(2)探究“镁粉”中是否还含有MgO及Mg(OH)2.
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验,分别取0.5g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失,在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
Mg(OH)2与盐酸发生中和反应的化学方程式为Mg(OH)2+2HCl═MgCl2+2H2O.
Ⅱ.取“镁粉”样品0.5g,加入上述稀盐酸至粉末恰好溶解,此时消耗稀盐酸的体积约为5.3mL.
【实验分析及结论】
“镁粉”不只含有MgCO3,理由是0.5gMgCO3消耗的盐酸体积与0.5g“镁粉”消耗的盐酸体积不相等.
【实验反思】
为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL,由此可知“镁粉”中含有MgCO3的质量分数为85%,“镁粉”中除MgCO3外的另一种物质为Mg(OH)2.

已知:MgO+2HCl═MgCl2+H2O MgCO3+2HCl═MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3.
①取少量样品,如图1所示进行实验,观察到a试管中有气泡产生,b试管中产生的现象是澄清石灰水变浑浊,则证明“镁粉”中一定含有MgCO3.
②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭,但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成浓NaOH溶液,目的是除掉二氧化碳.小明按照修改后的实验方案重复上述实验,观察到b试管口,证明“镁粉”中不含Mg.
(2)探究“镁粉”中是否还含有MgO及Mg(OH)2.
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验,分别取0.5g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失,在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
| MgO | Mg(OH)2 | MgCO3 | |
| 消耗稀盐酸的体积/mL | 10.4 | 7.2 | 5.0 |
Ⅱ.取“镁粉”样品0.5g,加入上述稀盐酸至粉末恰好溶解,此时消耗稀盐酸的体积约为5.3mL.
【实验分析及结论】
“镁粉”不只含有MgCO3,理由是0.5gMgCO3消耗的盐酸体积与0.5g“镁粉”消耗的盐酸体积不相等.
【实验反思】
为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL,由此可知“镁粉”中含有MgCO3的质量分数为85%,“镁粉”中除MgCO3外的另一种物质为Mg(OH)2.