题目内容
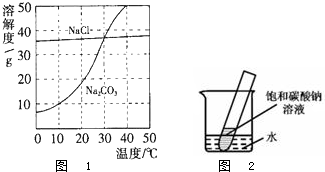
如图1为元周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥原子径由大到小的顺序是 .
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是 .
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: .
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号) .
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生如图2的反应,X溶液与Y溶液反应的离子方程式为 ,N-→⑥的单质的化学方程式为 ,常温下,为使0.1mol/L M溶液中由M电离的阴阳离子浓度相等,应向溶液中加入一定量的Y溶液至 .

(1)④、⑤、⑥原子径由大到小的顺序是
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生如图2的反应,X溶液与Y溶液反应的离子方程式为

考点:元素周期表的特点及其应用,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:(1)根据电子层越多半径越大,电子层一样多的原子,核电荷数越多半径越小进行解答;
(2)根据同一周期元素的原子,从左到右最高价氧化物对应水化物的酸性逐渐增强进行解答;
(3)根据过氧化钠是既含离子键又含共价键的化合物进行解答;
(4)根据二氧化锰或氯化铁都能作过氧化氢溶液反应的催化剂进行解答;
(5)根据M是仅含非金属的盐所以一定是铵盐;Z
N→⑥的单质.根据周期表的结构判断⑥是金属铝,所以推断N是氧化铝,Z是氢氧化铝,分析产物结合反应:X+Y+H2O→Al(OH)3+NH4+可知XY是铝盐和一水合氨的反应进行解答.
(2)根据同一周期元素的原子,从左到右最高价氧化物对应水化物的酸性逐渐增强进行解答;
(3)根据过氧化钠是既含离子键又含共价键的化合物进行解答;
(4)根据二氧化锰或氯化铁都能作过氧化氢溶液反应的催化剂进行解答;
(5)根据M是仅含非金属的盐所以一定是铵盐;Z
| 加热 |
解答:解:根据元素在周期表中的分布,可以知道①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是Cl;
(1)电子层越多半径越大,所以Na、Al>O,电子层一样多的原子,核电荷数越多半径越小,即Na>Al;故答案为:Na>Al>O;
(2)②③是C、N,是同一周期元素的原子,根据元素周期律:从左到右最高价氧化物对应水化物的酸性逐渐增强,所以酸性:HNO3>H2CO3,②⑦是C、Si,是同主族元素,根据元素周期律:从上到下最高价氧化物对应水化物的酸性逐渐减弱,H2CO3>H2SiO3;故答案为:HNO3>H2CO3>H2SiO3;
(3)①④⑤⑧分别是H、O、Na、Cl,其中钠元素、氧原子、氢元素组成的氢氧化钠,钠元素、氧原子、氯元素组成的次氯酸钠,均是既含离子键又含极性共价键的化合物,电子式为:,Na+ ;故答案为:Na+
;故答案为:Na+ ;
;
(4)二氧化锰或氯化铁都能作过氧化氢溶液反应的催化剂;故选:ab;
( )⑥的单质Al与⑤Na的最高价氧化物的水化物NaOH发生反应生成偏铝酸钠和氢气,化学方程式为:2Al+2NaOH+2H2O=2NaOH+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaOH+3H2↑;
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生如图转化的反应,其中M是仅含非金属的盐,所以一定是铵盐;Z
N→⑥的单质.根据周期表的结构判断⑥是金属铝,所以推断N是氧化铝电解生成金属铝,Z是氢氧化铝受热分解生成氧化铝,分析产物结合反应:X+Y+H2O→Al(OH)3+NH4+ 可知XY是铝盐和一水合氨的反应;所以X溶液与Y溶液反应的离子方程式为:Al3++3NH3+3H2O=Al(OH)3↓+3NH4+;N-→⑥的单质的化学方程式为2Al2O3(熔融)
4Al+3O2↑;常温下,为使0.1mol/L M溶液中由M电离的阴阳离子浓度相等,应向溶液中加入一定量的Y溶液至中性,pH等于7.故答案为:Al3++3NH3+3H2O=Al(OH)3↓+3NH4+;2Al2O3(熔融)
4Al+3O2↑;溶液的pH等于7.
(1)电子层越多半径越大,所以Na、Al>O,电子层一样多的原子,核电荷数越多半径越小,即Na>Al;故答案为:Na>Al>O;
(2)②③是C、N,是同一周期元素的原子,根据元素周期律:从左到右最高价氧化物对应水化物的酸性逐渐增强,所以酸性:HNO3>H2CO3,②⑦是C、Si,是同主族元素,根据元素周期律:从上到下最高价氧化物对应水化物的酸性逐渐减弱,H2CO3>H2SiO3;故答案为:HNO3>H2CO3>H2SiO3;
(3)①④⑤⑧分别是H、O、Na、Cl,其中钠元素、氧原子、氢元素组成的氢氧化钠,钠元素、氧原子、氯元素组成的次氯酸钠,均是既含离子键又含极性共价键的化合物,电子式为:,Na+
 ;故答案为:Na+
;故答案为:Na+ ;
;(4)二氧化锰或氯化铁都能作过氧化氢溶液反应的催化剂;故选:ab;
( )⑥的单质Al与⑤Na的最高价氧化物的水化物NaOH发生反应生成偏铝酸钠和氢气,化学方程式为:2Al+2NaOH+2H2O=2NaOH+3H2↑,故答案为:2Al+2NaOH+2H2O=2NaOH+3H2↑;
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生如图转化的反应,其中M是仅含非金属的盐,所以一定是铵盐;Z
| 加热 |
| ||
| ||
点评:本题考查了元素周期表的结构、元素位置、规律变化的应用,主要依托常见元素及其化合物,分析比较原子半径大小,同周期同主族性质递变的应用,化学键的形成和存在,利用铝及其化合物的化学性质,金属铝的制备等知识推断物质.

练习册系列答案
相关题目
Fe、Fe2+、Fe3+相同的是( )
| A、核电荷数 | B、核外电子数 |
| C、化学性质 | D、所带电性 |
如表为某科学家通过研究获得的信息(“√”表示能够存活,“×”表示不能存活)根据所给信息,判断下列说法错误的是( )
| pH值范围 | 6.5-7.0 | 6.0-6.5 | 4.5-6.0 | 3.0-4.5 |
| 溪红点鲑 | √ | √ | × | × |
| 小口黑鲈 | √ | √ | × | × |
| 黑头呆鱼 | √ | × | × | × |
| 牛蛙胚胎 | √ | √ | √ | × |
| 小龙虾 | √ | √ | × | × |
| A、水体的pH值为3.0-4.5时,最适合这些生物生存 |
| B、该实验研究的是水体pH的变化对部分生物的影响 |
| C、上述生物中牛蛙胚胎在水体pH变化时存活范围最大 |
| D、水体pH发生变化可能是由于酸雨造成的 |