题目内容
化学实验小组的同学将一定量的Ca(OH)2溶液与Na2CO3溶液混合,充分反应后过滤.得到无色滤液,他们对滤液的成分进行探究.
【提出问题】滤液里可能含有哪些溶质呢?
【猜想与假设】甲同学猜想可能含有NaOH和Na2CO3;乙同学猜想可能含有NaOH、Na2CO3和Ca(OH)2;
丙同学猜想可能恰好完全反应只含NaOH;丁同学猜想可能含有 .
【实验验证】(1)请你对甲同学的猜想,设计一个简单的实验加以证明.
【物质鉴别】化学小组同学选用了两种不同类别的试剂进行实验,鉴别甲同学猜想,并得出结论--碳酸钠存在.请将鉴别的化学方程式填在表中.’
【提出问题】滤液里可能含有哪些溶质呢?
【猜想与假设】甲同学猜想可能含有NaOH和Na2CO3;乙同学猜想可能含有NaOH、Na2CO3和Ca(OH)2;
丙同学猜想可能恰好完全反应只含NaOH;丁同学猜想可能含有
【实验验证】(1)请你对甲同学的猜想,设计一个简单的实验加以证明.
| 实验步骤 | 实验现象 | 实验结论 |
| 甲同学的猜想成立 |
| 化学方程式 | |
| 试剂1 | |
| 试剂2 |
考点:实验探究物质的组成成分以及含量,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【猜想与假设】物质之间发生化学反应时,存在着一定的量的关系,即量的多少能直接影响物质之间是否恰好完全反应.本题中给出的一定量的Ca(OH)2溶液与Na2CO3溶液混合,并没有说明量的关系,因而存在三种情况:①恰好完全反应,药品无剩余,此时溶质仅有氢氧化钠;②碳酸钠量多,反应完有剩余,此时溶质有氢氧化钠和碳酸钠;③氢氧化钙量多,反应完有剩余,此时溶质有氢氧化钠和氢氧化钙.
【实验验证】(1)根据碳酸钠能够和氯化钙反应产生沉淀及氢氧化钠能够使酚酞试液变成红色分析.
【物质鉴别】根据碳酸钠的化学性质解答.
【实验验证】(1)根据碳酸钠能够和氯化钙反应产生沉淀及氢氧化钠能够使酚酞试液变成红色分析.
【物质鉴别】根据碳酸钠的化学性质解答.
解答:解:
【猜想与假设】
Na2CO3+Ca(OH)2=2NaOH+CaCO3;↓两种物质如果是恰好完全反应,则溶质只能是NaOH,如果有物质过量,则还可能含有Na2CO3或Ca(OH)2;,但是这两种物质只能有一种剩余,不可能同时剩余,Na2CO3或Ca(OH)2;
所以丁同学猜想的答案为:NaOH和Ca(OH)2;
【实验验证】甲同学猜想可能含有NaOH和Na2CO3,要设计实验加以证明,只需要证明有Na2CO3就可以了
因为猜想的物质中只有碳酸钠能够和氯化钙反应产生沉淀,因此根据现象产生白色沉淀,说明滤液中一定含有Na2CO3;
【物质鉴别】
甲同学猜想可能含有NaOH和Na2CO3,要设计实验加以证明,只需要证明有Na2CO3就可以了,并得出结论--碳酸钠存在,需要根据碳酸钠的性质选择试剂,且所选的试剂与碳酸钠发生化学反应得有明显的实验现象,例如产生沉淀或冒出气泡等,故本题答案为:
答案:
【猜想与假设】
NaOH和Ca(OH)2
【实验验证】取少量滤液于试管中,加入过量CaCl2溶液,充分反应后静置 有白色沉淀出现
【物质鉴别】
【猜想与假设】
Na2CO3+Ca(OH)2=2NaOH+CaCO3;↓两种物质如果是恰好完全反应,则溶质只能是NaOH,如果有物质过量,则还可能含有Na2CO3或Ca(OH)2;,但是这两种物质只能有一种剩余,不可能同时剩余,Na2CO3或Ca(OH)2;
所以丁同学猜想的答案为:NaOH和Ca(OH)2;
【实验验证】甲同学猜想可能含有NaOH和Na2CO3,要设计实验加以证明,只需要证明有Na2CO3就可以了
因为猜想的物质中只有碳酸钠能够和氯化钙反应产生沉淀,因此根据现象产生白色沉淀,说明滤液中一定含有Na2CO3;
【物质鉴别】
甲同学猜想可能含有NaOH和Na2CO3,要设计实验加以证明,只需要证明有Na2CO3就可以了,并得出结论--碳酸钠存在,需要根据碳酸钠的性质选择试剂,且所选的试剂与碳酸钠发生化学反应得有明显的实验现象,例如产生沉淀或冒出气泡等,故本题答案为:
| 试剂1 | Na2CO3+Ca(OH)2═CaCO3↓+2NaOH |
| 试剂2 | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
【猜想与假设】
NaOH和Ca(OH)2
【实验验证】取少量滤液于试管中,加入过量CaCl2溶液,充分反应后静置 有白色沉淀出现
【物质鉴别】
| 试剂1 | Na2CO3+Ca(OH)2═CaCO3↓+2NaOH |
| 试剂2 | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
点评:本题综合考查了酸碱盐之间的复分解反应,以及量的关系导致物质剩余的猜测,属于难度较大的题目.要完成此类题目,需要熟练掌握酸碱盐的化学性质,以及相互之间发生的化学反应和所产生的实验现象.

练习册系列答案
相关题目
通过燃烧除去密闭容器中空气中的氧气,且不产生其它气体,可选用的物质是( )
| A、铁 | B、蜡烛 | C、木炭 | D、红磷 |

 如图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题:
如图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题: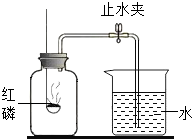 为测定空气里氧气的含量,甲、乙、两个同学用如图的装置分别进行了实验探究.
为测定空气里氧气的含量,甲、乙、两个同学用如图的装置分别进行了实验探究.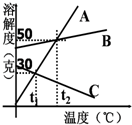 A、B、C三种物质的溶解度随温度的变化情况如图:
A、B、C三种物质的溶解度随温度的变化情况如图: