题目内容
9.120t含氧化铁80%的赤铁矿石中含铁元素的质量为67.2t.分析 根据题干中赤铁矿与氧化铁的关系,求出氧化铁的质量;
根据物质中某元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{化合物的相对分子质量}$×100%.即可求铁元素的质量.
解答 解:1000吨含氧化铁80%的赤铁矿中含氧化铁的质量为:120t×80%=96t
氧化铁中铁元素的质量分数=$\frac{56×2}{160}$×100%
96t氧化铁中含铁元素的质量为:96t×$\frac{56×2}{160}$×100%=67.2t
故答案为:67.2
点评 本题考查学生对物质中某元素的质量的计算方法的掌握,计算时要理清各个量之间的关系,再结合题意进行分析解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19. 2016年1月6日,朝鲜宣布第一枚氢弹成功试验,引起国际社会的关注.引爆氢弹极为困难,引爆需要在氢弹内部安放小型原子弹,瞬间达到反应条件温度,而原子弹中含铀元素(部分信息如图所示).下列有关铀说法错误的是( )
2016年1月6日,朝鲜宣布第一枚氢弹成功试验,引起国际社会的关注.引爆氢弹极为困难,引爆需要在氢弹内部安放小型原子弹,瞬间达到反应条件温度,而原子弹中含铀元素(部分信息如图所示).下列有关铀说法错误的是( )
 2016年1月6日,朝鲜宣布第一枚氢弹成功试验,引起国际社会的关注.引爆氢弹极为困难,引爆需要在氢弹内部安放小型原子弹,瞬间达到反应条件温度,而原子弹中含铀元素(部分信息如图所示).下列有关铀说法错误的是( )
2016年1月6日,朝鲜宣布第一枚氢弹成功试验,引起国际社会的关注.引爆氢弹极为困难,引爆需要在氢弹内部安放小型原子弹,瞬间达到反应条件温度,而原子弹中含铀元素(部分信息如图所示).下列有关铀说法错误的是( )| A. | 属于金属元素 | B. | 相对原子质量为238.0g | ||
| C. | 原子的核电荷数是92 | D. | 该元素的核外电子数为92 |
20.如图为甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )
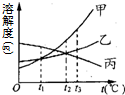

| A. | 在t1℃时,溶解度甲=乙<丙 | |
| B. | 从乙饱和溶液中析出较多量的晶体通常可采用降温结晶法 | |
| C. | 等质量的甲、乙饱和溶液从t3℃降温到t1℃,析出晶体(无结晶水)的质量甲>乙 | |
| D. | t2℃时,将乙、丙的饱和溶液升温至t3℃,乙溶液的溶质质量分数增大,丙溶液的溶质质量分数减小 |
4.下列有关说法正确的是( )
| A. | 含氧元素质量分数最高的氧化物是水 | |
| B. | 空气是一种重要的自然资源,它是由氧气和氮气两种气体组成的 | |
| C. | 地球上的水资源是丰富的,但可利用的淡水资源只约占全球水储量的2.53% | |
| D. | 海洋中含有80多种元素,其中含量最多的金属元素是钠元素 |
18.下列说法正确的是( )
| A. | 煤气泄漏,用明火查看 | B. | 明矾净水,能杀菌消毒 | ||
| C. | 油锅着火,可加水浇灭 | D. | 金属回收,可节能防污 |
 碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.