题目内容
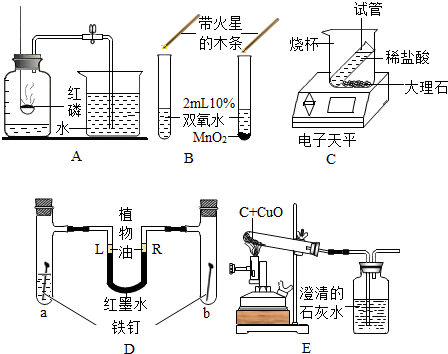
14.根据如图所示实验,请回答相关问题:(1)图A中若红磷用量不足,测得空气中氧气的体积分数将偏小(填写“偏大”、“偏小”或“无影响”).
(2)图B中实验运用了控制变量,对照实验的研究方法,二氧化锰在反应前后质量与化学性质均不改变.
(3)图C中反应后天平示数减小,有人说该反应不符合质量守恒定律,你的观点是符合质量守恒定律,反应后产生的气体未被称量到,所以反应后质量减少.
(4)图D是探究铁锈蚀的条件的实验装置,a管中装入少量煮沸的蒸馏水,b管中是干燥的空气,调节L端与R端的液面一致,塞紧木塞,一周后观察,该实验可以说明铁的锈也需要水.
(5)图E中的不足之处是没有尾气处理装置.
分析 (1)根据实验原理分析误差;
(2)根据实验对比结合催化剂的特点分析;
(3)根据质量守恒定律的内容分析;
(4)根据已有的知识进行分析,铁在与水和氧气并存时易生锈,据此解答.
(5)根据一氧化碳有毒来分析.
解答 解:(1)若红磷不足,就不能把氧气完全消耗,因此结果会偏小;故填:偏小;
(2)图B通过等体积等浓度的过氧化氢加二氧化锰能够加快反应的速率,是通过控制变量,对照实验得出结论;二氧化锰是过氧化氢分解的催化剂,因此反应前后质量与化学性质都不变;故填:控制变量,对照实验;质量与化学性质;
(3)装置C中将盐酸与大理石混合,反应停止后,天平不平衡,因为盐酸与碳酸钙反应生成二氧化碳气体,逸入空气,因此质量减少;
故填:符合质量守恒定律,反应后产生的气体未被称量到,所以反应后质量减少;
(4)铁制品被锈蚀都是由于铁直接与氧气和水接触造成的,因此a管内铁钉生锈,b管中铁钉放在干燥空气中不会生锈,从而使a管气体压强小于b管,L端液面会上升,故填:水;
(5)在反应中可能会生成有毒的一氧化碳气体,造成空气污染,应该进行尾气的处理,故填:没有尾气处理装置.
点评 此题难度不大,但综合性较强,掌握常见实验的现象、注意事项等是顺利解题的关键所在.

练习册系列答案
相关题目
5.如图表示治理汽车尾气所涉及反应的微观过程.下列说法不正确的是( )


| A. | 图中所示单质的化学式为N2 | |
| B. | 生成的单质与化合物的质量比为7:11 | |
| C. | 反应后分子个数变少了 | |
| D. | 图中所示有三种氧化物的分子 |
19.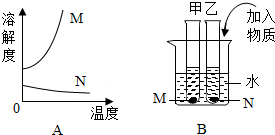 A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,加入的物质可能是( )
A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,加入的物质可能是( )
 A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,加入的物质可能是( )
A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,加入的物质可能是( )| A. | 冰水 | B. | NH4NO3 | C. | NaCl | D. | NaOH |
 如图是a、b、c三种物质的溶解度曲线:
如图是a、b、c三种物质的溶解度曲线: