题目内容
10.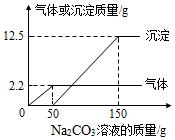 在实验课上,同学们用锌和稀硫酸反应制取氢气,小明取反应后的溶液164.7g,滴入碳酸钠溶液,先后有气体和白色沉淀生成,加入碳酸钠溶液与生成沉淀或气体的质量关系如图.
在实验课上,同学们用锌和稀硫酸反应制取氢气,小明取反应后的溶液164.7g,滴入碳酸钠溶液,先后有气体和白色沉淀生成,加入碳酸钠溶液与生成沉淀或气体的质量关系如图.(1)滴入碳酸钠溶液后,生成的气体是CO2;
(2)碳酸钠溶液中碳酸钠的质量分数为10.6%;(计算结果精确到0.1%,下同)
(3)当加入150g碳酸钠溶液时,所得溶液中溶质的质量分数为多少?((3)写出计算过程)
分析 (1)根据碳酸钠分别与硫酸反应生成二氧化碳、与硫酸锌反应生成碳酸锌沉淀分析;
(2)分别利用氢气的质量和沉淀的质量根据化学方程式计算出参加反应的碳酸钠的质量,再求和,进而求质量分数;
(3)分别利用氢气的质量和沉淀的质量根据化学方程式计算出生成的硫酸钠的质量,再求质量分数.
解答 解:(1)发生的反应有:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,Na2CO3+ZnSO4=ZnCO3↓+Na2SO4,则生成的气体是二氧化碳;故答案为:CO2;
设硫酸反应消耗碳酸钠的质量为x,生成硫酸钠的质量为y;硫酸锌反应消耗碳酸钠的质量为m,生成硫酸钠的质量为n.
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 142 44
x y 2.2g
则$\frac{106}{x}=\frac{142}{y}=\frac{44}{2.2g}$,解得x=5.3g,y=7.1g.
Na2CO3+ZnSO4=ZnCO3↓+Na2SO4
106 125 142
m 12.5g n
则$\frac{106}{m}=\frac{125}{12.5g}=\frac{142}{n}$,解得m=10.6g,n=14.2g.
(2)碳酸钠溶液中碳酸钠的质量分数为:$\frac{5.3g}{50g}×100%$=10.6%
答:碳酸钠溶液中碳酸钠的质量分数为10.6%;
(3)反应后溶液的质量:164.7g+150g-2.2g-12.5g=300g,硫酸钠的质量分数:$\frac{7.1g+14.2g}{300g}$×100%=7.1%
答:所得溶液中硫酸钠的质量分数为7.1%.
点评 本题主要考查含杂质物质的化学方程式计算和溶质质量分数的计算,增加了学生分析问题的思维跨度,考查了学生整合知识的能力,要明确该题中发生反应的过程,理清思路是解决该题的关键,有一定难度.

①滤渣中一定含有锌
②滤渣中一定含有铜,可能含有锌
③向滤渣中加入稀盐酸,最后溶液一定变成浅绿色
④滤液中溶质一定含有硫酸锌和硫酸镁
⑤滤液的颜色不可能为浅绿色
以上说法中正确的是( )
| A. | ①③④ | B. | ②③⑤ | C. | ②④ | D. | ①④⑤ |
| A. | 电解水实验得到氢气和氧气能说明水是由氢、氧两种元素组成的化合物 | |
| B. | 氢氧化钠与硫酸铜溶液反应前后质量测定实验能说明化学变化遵循质量守恒定律 | |
| C. | 黄豆与芝麻混合的实验能说明分子之间有空隙 | |
| D. | 二氧化碳灭火实验能说明二氧化碳不助燃、不可燃、密度大于空气 |
| A. | 干冰升华 | B. | 金属生锈 | C. | 高炉炼铁 | D. | 食物变质 |
| A. | C→CO2→O2 | B. | Cu→CuO→CuSO4 | ||
| C. | Na2CO3→NaNO3→NaCl | D. | Fe→FeCl2→AgCl |
(一)张林同学用物理方法鉴别它们.他从两瓶溶液中各取出来少许分别装入试管并在酒精灯火焰上加热.他根据甲中溶液变浑浊现象,判断甲瓶为石灰水.
(二)李莉同学用化学方法鉴别它们.她从两瓶溶液取出来少许装入试管并向里面吹气,也判断出甲瓶为石灰水,她看到现象的化学反应方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
(三)乙瓶溶液敞放在空气中可能变质.为了探究乙瓶是否变质?以及变质后溶液中溶质的成分?两位同学做了如下猜测和实验.
【提出猜想】:①只有NaOH ②只有Na2CO3 ③Na2CO3和NaOH ④…
【查阅资料】:已知NaCl、CaCl2溶液呈中性,Na2CO3溶液能使酚酞变红.
【实验与结论】:
(1)取少许溶液并加入氢氧化钙溶液,看不到任何现象就可证明猜想①成立.
(2)若氢氧化钠溶液已经变质,要探究氢氧化钠溶液是否完全变质,他们做了如下实验.
| 实验步骤 | 实验现象 | 实验结论或方程式 |
| 步骤1:取少量已变质的NaOH溶液于试管中,加入过量的氯化钙溶液 | 产生白色沉淀 | 反应方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl. |
| 步骤2:取步骤1所得的澄清溶液少许,并向清液滴入几滴酚酞. | 红色 | 猜想③成立 |
| A. | KNO3是一种复合肥 | |
| B. | 农药施用后,会通过农作物和农产品积累、转移 | |
| C. | 为了保证高产,尽量多施用农药、化肥 | |
| D. | 观察颜色可区别氯化钾和磷矿粉 |
 能源、环境与人类社会密切相关.下面关于几种常见的新能源:
能源、环境与人类社会密切相关.下面关于几种常见的新能源: