题目内容
18.【碱石灰是氢氧化钠和氧化钙的混合物】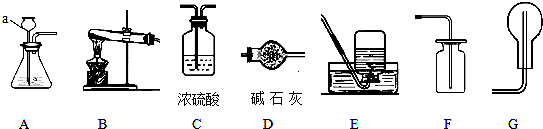
(1)写出图中标有字母的仪器的名称:a为长颈漏斗.
(2)分别写出实验室用A装置制取氧气和二氧化碳的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑、CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)氨气是一种无色、有刺激性气味的气体,极易溶于水,氨水显碱性.实验室用加热氯化铵和熟石灰两种固体的混合物来制取氨气,实验室制取、干燥、收集氨气的装置应分别选用(填序号)B、D、G.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据石灰石和稀盐酸反应原理、双氧水制取氧气的反应原理进行分析;
(3)根据反应及气体的性质,确定发生和收集装置;干燥气体时注意干燥剂的选用--既能吸收水分又不与气体发生反应.
解答 解:(1)通过分析题中所指仪器的作用可知,a为长颈漏斗;
(2)实验室制取CO2的反应物是碳酸钙与稀盐酸,生成物是氯化钙、水、二氧化碳,化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;双氧水制取氧气的反应原理是过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)加热固体氯化铵和熟石灰制取氨气,发生装置应选B;氨气“极易溶于水”,不能用排水法收集,其密度可通过计算相对分子质量来判断:14+1×4=18(18<29),密度比空气小,应用向下排空气法收集;氨水呈碱性,干燥时不能选用浓硫酸作干燥剂;故选B、D、G.
故答案为:(1)长颈漏斗;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)B,D,G.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
8.下列叙述,你认为科学的是( )
| A. | 洗涤剂去除油污是因为洗涤剂可以溶解油污 | |
| B. | 钢丝球洗刷铝制炊具 | |
| C. | 霉变大米加热后可食用 | |
| D. | 减少使用塑料制品可以减少白色污染 |
6.蔗糖(C12H22O11)在甜菜、甘蔗中含量极高.下列有关C12H22O11的说法正确的是( )
| A. | C12H22O11属于氧化物 | |
| B. | 一个蔗糖分子中碳原子的质量为144g | |
| C. | C12H22O11中氢元素的质量分数最大 | |
| D. | C12H22O11中氢、氧原子的个数比为2:1 |
13.如图分别是铝元素、氯元素的原子结构示意图.下列叙述正确的是( )
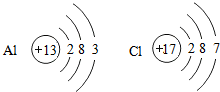

| A. | 铝原子第一电子层有3个电子 | B. | 氯原子核内有17个质子 | ||
| C. | 氯原子在化学反应中容易失去电子 | D. | 铝原子核带13个单位负电荷 |
3.下列物质中碳元素的化合价为+4的是( )
| A. | C | B. | CO | C. | CO2 | D. | CH4 |
7.维生素C(化学式为C6H8O6)是人体不可缺少的营养物质.下列关于维生素C的叙述正确的是( )
| A. | 是氧化物 | |
| B. | 氧元素的质量分数计算式为$\frac{6}{176}$×100% | |
| C. | 每个分子中含有20个原子 | |
| D. | 碳、氢、氧三种元素的质量比3:4:3 |