题目内容
4.国家规定,酿造食醋总酸含量不得低于3.5g/100mL(总酸含量即100mL食醋中含醋酸的质量).某兴趣小组为测定一市售食用白醋的总酸含量,进行了如下实验:首先取10mL该白醋样品;然后用溶质质量分数为0.4%的NaOH溶液中和,当消耗NaOH溶液75g时,恰好完全反应(醋酸与氢氧化钠反应的化学方程式为:CH3COOH+NaOH═CH3COONa+H2O,假设其他物质不与氢氧化钠反应).
计算:该市售白醋样品中的总酸含量,并说明是否符合国家标准.
分析 根据氢氧化钠溶液的质量、溶质质量分数可以计算醋酸的质量,进一步可以判断该市售白醋样品是否符合国家标准.
解答 解:设醋酸的质量为x,
氢氧化钠的质量为:75g×0.4%=0.3g,
CH3COOH+NaOH═CH3COONa+H2O,
60 40
x 0.3g
$\frac{60}{x}$=$\frac{40}{0.3g}$,
x=0.45g,
即10mL样品中含有0.45g醋酸,因此100mL样品中的总酸含量为4.5g/100mL,
因为4.5g/100mL>3.5g/100mL,
所以符合国家标准.
答:该市售白醋样品中的总酸含量是4.5g/100mL,符合国家标准.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
12.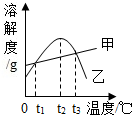 甲、乙两种物质固体的溶解度曲线如右图所示,下列有关说法正确的是( )
甲、乙两种物质固体的溶解度曲线如右图所示,下列有关说法正确的是( )
 甲、乙两种物质固体的溶解度曲线如右图所示,下列有关说法正确的是( )
甲、乙两种物质固体的溶解度曲线如右图所示,下列有关说法正确的是( )| A. | 乙的溶解度随温度的升高而增大 | |
| B. | 乙和甲的饱和溶液从t3℃降温到t2℃均有晶体析出 | |
| C. | t2℃时,乙溶液的溶质质量分数一定大于甲溶液 | |
| D. | 随着温度的降低,甲饱和溶液的容质质量的分数逐渐降低 |
19.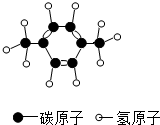 近年来,因建设“PX”项目而引发的争议时有发生.PX是一种重要的化工原料,化学名称为对二甲苯,其分子结构模型如图所示.下列有关“PX”的叙述不正确的是( )
近年来,因建设“PX”项目而引发的争议时有发生.PX是一种重要的化工原料,化学名称为对二甲苯,其分子结构模型如图所示.下列有关“PX”的叙述不正确的是( )
 近年来,因建设“PX”项目而引发的争议时有发生.PX是一种重要的化工原料,化学名称为对二甲苯,其分子结构模型如图所示.下列有关“PX”的叙述不正确的是( )
近年来,因建设“PX”项目而引发的争议时有发生.PX是一种重要的化工原料,化学名称为对二甲苯,其分子结构模型如图所示.下列有关“PX”的叙述不正确的是( )| A. | “PX”是一种有机物 | |
| B. | “PX”的化学式为C8H10 | |
| C. | “PX”中C、H元素的质量比为4:5 | |
| D. | “PX”中碳元素的质量分数约为90.6% |
16.如表是小乐同学制作的化学知识卡片的部分内容,请将其补充完整.
| 序号 | 专题:物质的类别、性质和用途 | 整理时间:2015年3月 | ||
| 物质 | 类别 | 性质 | 对应的用途 | |
| (1) | 酒精 | 有机物 | 可燃性 | 做燃料 |
| (2) | 氢氧化钠 | 碱 | 吸水性 | 干燥剂 |
| (3) | 一氧化碳 | 氧化物 | 还原性 | 冶炼金属 |
| (4) | 石墨 | 单质 | 导电性 | 做电极 |
14.每到冬天,市场上便有一种“热宝”出售,其化学成分主要包括铁粉、碳粉和少量氯化钠.小明用“热宝”中的物质完成如下实验,其中实验操作及现象与结论一一对应的是( )
| 选项 | 实验操作 | 实验结论 |
| A | 取适量样品于布袋内,揉搓数次至手感觉发烫 | 只发生了物理变化 |
| B | 取适量样品于试管中,滴入适量盐酸,有气泡产生 | “热宝”中含有铁 |
| C | 取适量样品放在足量O2中燃烧 | 剩余固体只有Fe3O4 |
| D | 取适量样品加入到盛有一定量的CuSO4溶液的烧杯中,充分反应后,过滤 | 滤液中的溶质为FeSO4 |
| A. | A | B. | B | C. | C | D. | D |
 2014年9月第18届省运会在我市举办,精彩的盛会给人们留下了深刻的印象.
2014年9月第18届省运会在我市举办,精彩的盛会给人们留下了深刻的印象.