题目内容
20.化学与生产、生活实际密切相关.(1)如表是某品牌饼干的营养成分.由此可知该饼干缺少的营养素是维生素、水.
| 蛋白质 | 脂肪 | 糖类 | 钠 | 钙 |
| 10克 | 20克 | 61克 | 693毫克 | 300毫克 |

(3)2009年哥本哈根气候大会召开之际,“低碳”也再次成为各方关注的焦点.低碳生活其实就在身边:每节约1度电,就可以减排1千克二氧化碳;少用10双一次性筷子,减排0.2千克….下列生活习惯符合低碳生活的是ABC(填字母).
A、植树种草B、作业本双面使用C、用太阳能沐浴代替电热水器
(4)青少年成长必须吸收足够的“钙”,若人体缺钙可能引起BDE(填字母).
A.贫血 B.佝偻病 C.坏血病 D.骨质疏松 E. 软骨病
(5)淀粉不仅是食物中的营养素,而且通过发酵可生产乙醇(C2H5OH),现已推广为汽车的清洁燃料--乙醇汽油.乙醇完全燃烧的化学方程式C2H5OH+3O$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O..
分析 (1)根据人体所需六大营养素的种类,结合题中所给的营养成分判断所含的营养素以及缺少的营养素.
(2)根据材料的分类进行分析解答.
(3)“低碳生活”指的是生活作息时所耗用的能量要尽量减少,特别是减少二氧化碳的排放量,减缓生态恶化;可以从节电、节能和回收等环节来改变生活细节,据此进行分析解答即可.
(4)根据钙的生理功能和缺乏症进行分析判断.
(5)乙醇燃烧生成二氧化碳和水,写出反应的化学方程式即可.
解答 解:(1)人体需要的六大营养物质:蛋白质、糖类、油脂、维生素、无机盐和水;结合题意,该饼干含有蛋白质、糖类、油脂、无机盐,缺少维生素、水.
(2)A、鸟巢的钢结构属于金属材料;B、自清洁塑料属于合成有机高分子材料;C、汉白玉属于无机材料;D、汽车轮胎属于合成有机高分子材料.
(3)A、植树种草,增大绿化面积,树木、花草可以通过光合作用吸收二氧化碳,故选项符合“低碳生活”理念.
B、作业本双面使用,可以减少植物的消耗,故选项符合“低碳生活”理念.
C、用太阳能沐浴代替电热水器,可以减少二氧化碳的排放,故选项符合“低碳生活”理念.
(4)钙主要存在于骨胳和牙齿中,使骨和牙齿具有坚硬的结构支架,缺乏幼儿和青少年会患佝偻病、软骨病,老年人会患骨质疏松.
(5)乙醇燃烧生成二氧化碳和水,反应的化学方程式为C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$ 2CO2+3H2O.
故答案为:(1)维生素、水;(2)BD;(3)ABC;(4)BDE;(5)C2H5OH+3O$\frac{\underline{\;点燃\;}}{\;}$ 2CO2+3H2O.
点评 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.

| A. | 纯水是中性的,所以它的pH等于7 | |
| B. | 银跟盐酸起反应,生成氯化银和氢气 | |
| C. | 混有水蒸气的CO2通过NaOH固体后,得到干燥的CO2 | |
| D. | 凡能电离产生OH-离子的化合物叫做碱 |
| A. | 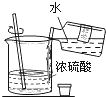 稀释浓硫酸 | B. | 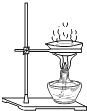 蒸发食盐水 | ||
| C. |  套橡胶管 | D. | 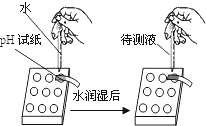 测溶液pH |
| A. | 向上排空气法 | B. | 向下排空气法 | ||
| C. | 排水法 | D. | 排水法或向上排空气法 |
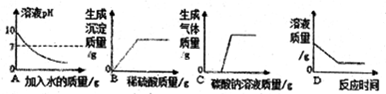
| A. | 常温下向pH=10的NaOH溶液不断加入水稀释 | |
| B. | 向一定量的氢氧化钠和氯化钡的混合溶液中滴加稀硫酸 | |
| C. | 向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| D. | 向一定质量的饱和石灰水中加过量的生石灰 |
| A. |  制取、收集氧气 | B. |  蒸发结晶 | ||
| C. |  检查装置气密性 | D. |  熄灭酒精灯 |
【查阅资料】过氧化钠能与空气中水和二氧化碳反应生成氧气:
2Na2O2+2H2O=4NaOH+O2↑,2Na2O2+2CO2═2Na2CO3+O2.
【提出问题】过氧化钠是否变质?
【猜想与假设】假设1:过氧化钠未变质;
假设2:过氧化钠部分变质;
假设3:过氧化钠全部变质.
【实验探究】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解, 木条复然 | 假设3 不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的稀盐酸,振荡. | 有气泡生成 | 假设2成立 |
【实验探究】③取少量①中溶液于试管中,加人足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】
(1)由实验③可以确定①中溶液含有的溶质是NaOH、Na2CO3(填化学式);
(2)小明认为,由上述实验无法确定原固体样品中是否含有氢氧化钠,理由是过氧化钠与水反应能生成氢氧化钠,不能说明原来是否存在.
【定量研究】
称取6.04g过氧化钠药品于锥形瓶中,加入适量蒸馏水使固体完全溶解,共收集到0.64g气体;再向上述锥形瓶中加入足量的澄清石灰水,充分反应,经过滤、干燥等操作,称量固体质量为2.00g.
(1)写出加入澄清石灰水发生反应的化学方程式:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(2)6.04g上述样品中含有NaOH的质量为0.8g.
【反思提高】
过氧化钠长时间露置在空气中会全部变质,最终转化为Na2CO3(填化学式).
| A. | 尿素CO(NH2)2 | B. | 磷矿粉Ca2(PO4)2 | ||
| C. | 硫酸钾K2SO4 | D. | 磷酸二氢铵NH4H2PO4 |