题目内容
11.下列各组物质分别加入到足量的水中,最终能得到无色、透明溶液的是( )| A. | NaOH NaCl KNO3 MgCl2 | B. | NaOH Na2CO3 NaCl H2SO4 | ||
| C. | NaCl Na2SO4 AgNO3 HNO3 | D. | FeSO4 NaNO3 KCl HCl |
分析 本题考查利用复分解反应的条件来判断常见物质间的反应及溶解性规律,若物质之间相互交换成分,能结合成沉淀的则不能得到透明的溶液;本题还要注意能得到无色透明溶液,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:A、氢氧化钠能与氯化镁反应生成氢氧化镁沉淀,不透明,故错误;
B、三者之间不反应,且都是无色透明溶液,故此选项正确;
C、氯化钠与硝酸银反应生成氯化银是沉淀,不透明,故此选项错误;
D、三者之间不反应,但硫酸亚铁溶于水呈浅绿色,故此选项错误;
故选B.
点评 本题主要考查了离子的共存和溶液的带色问题,难度不是很大,对于能否得到无色透明的溶液,要注意彼此之间不能生成沉淀,还要注意特定离子的颜色,因此熟练掌握常见物质的溶解性规律及特殊离子的颜色是解题的关键.

练习册系列答案
相关题目
1.配制50g质量分数为6%的氯化钠溶液,不需要用到的仪器是( )
| A. | 托盘天平 | B. | 漏斗 | C. | 烧杯 | D. | 量筒 |
19.下列实验设计中不能达到实验目的是( )
| 实验设计 | 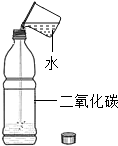 |  |  |  |
| 实验目的 | 验证二氧化碳与水反应生成碳酸 | 探究水的组成 | 证明石墨有导电性 | 验证氢气的密度比空气小 |
| 选项 | A | B | C | D |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
6.在购买和使用化肥时,要了解化肥的性质,以便合理施用,为了给农民做技术指导,小刚利用自己掌握的知识对碳酸钾(K2CO3)、硫酸铵[(NH4)2SO4]两种化肥的相关性质做了以下探究:
【实验探究】完成下列各题
【结论与应用】(5)碳酸钾与硫酸铵不能(填“能”或“不能”)混用,说明原因碳酸钾溶液呈碱性,与硫酸铵混合施用,产生NH3,降低肥效.
【知识拓展】(6)鉴别失去标签的碳酸钾和硫酸铵固体,下列试剂不可能的是C.
A.水 B.稀盐酸 C.氯化钡溶液 D.无色酚酞溶液.
【实验探究】完成下列各题
| 探 究 过 程 | 实 验 现 象 | 结论及化学方程式 | |
| K2CO3 | (NH4)2SO4 | ||
| (1)配制碳酸钾、硫酸铵溶液.分别取碳酸钾和硫酸铵固体,加足量水搅拌. | 得到澄清溶液,温度无明显变化 | 得到澄清溶液,温度明显降低 | 都易溶于水,硫酸铵溶于水时吸收的热量大于放出的热量. |
| (2)猜想与假设. 碳酸钾、硫酸铵溶液的酸碱性都可能有三种情况. 分别取少量两种溶液于两只试管中,滴加紫色石蕊试液. | 变蓝 | 变红 | 说明碳酸钾溶液显碱性; 说明硫酸铵溶液显 酸 性. |
| (3)与盐酸反应. 分别像两只试管中加入稀盐酸. | 有气泡产生 | 无明显现象 | 写出相关的化学方程式2HCl+K2CO3=2=KCl+CO2↑+H2O. |
| (4)与氢氧化钠溶液反应. 分别向两种溶液中加入氢氧化钠溶液. | 无明显现象 | 产生白色沉淀、有刺激性气味的气体生成 | (NH4)2SO4+2NaOH═Na2SO4+2H2O+2NH3↑ |
【知识拓展】(6)鉴别失去标签的碳酸钾和硫酸铵固体,下列试剂不可能的是C.
A.水 B.稀盐酸 C.氯化钡溶液 D.无色酚酞溶液.
16.实验桌上现有包白色粉末,可能是氢氧化钠、硫酸钠、碳酸钠和氯化铜的两种或两种以上组成.现将其放入一干净的烧杯M中,加入足量的水后,固体全部溶解得到无色溶液,再滴加几滴无色酚酞,溶液变为红色.
为进一步确定白色粉末的成分,同学们进行了如下探究.
【查阅资料】碳酸钠溶液呈碱性;氯化钡溶液和硫酸钠溶液呈中性.
【讨论猜想】进过分析,针对白色粉末的组成,大家提出如下猜想:
小红:氢氧化钠、硫酸钠; 小华:氢氧化钠、碳酸钠;
小明:碳酸钠、硫酸钠; 小亮:氢氧化钠、碳酸钠和硫酸钠.
【实验探究】四位同学共同设计并进行了如下实验:
实验完毕后,同学们将试管A、B中的物质倒在同一烧杯中,然后过滤,滤液中除酚酞外一定还含有的溶质有HCl和NaCl.
为进一步确定白色粉末的成分,同学们进行了如下探究.
【查阅资料】碳酸钠溶液呈碱性;氯化钡溶液和硫酸钠溶液呈中性.
【讨论猜想】进过分析,针对白色粉末的组成,大家提出如下猜想:
小红:氢氧化钠、硫酸钠; 小华:氢氧化钠、碳酸钠;
小明:碳酸钠、硫酸钠; 小亮:氢氧化钠、碳酸钠和硫酸钠.
【实验探究】四位同学共同设计并进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取烧杯M中的少量溶液于试管A中,向其中加入一定量的稀盐酸 | 溶液由红色变为无色且有气泡产生. | 小红 的猜想不正确 |
| 2.另取烧杯M中的少量溶液于另一试管B中,向其中加入过量氯化钡溶液. | 出现白色沉淀 | 小亮的猜想正确 |
| 3.继续向试管B中加入过量的稀盐酸 | 沉淀一部分消失,并生成气泡 |
3.为测定某BaCl2溶液的溶质质量分数,进行如下实验:取104g该溶液于烧杯中,加入1g稀硝酸溶液酸化,无任何现象,然后将30g一定溶质质量分数的硫酸溶液分三次加入,每次充分反应后过滤、称量(实验中物质的质量损失忽略不计),数据如表:
根据以上数据计算:(BaCl2+H2SO4═BaSO4↓+2HCl)
(1)该实验过程中产生沉淀的总质量为23.3g.
(2)该BaCl2溶液中溶质的质量分数(写出计算过程)
| 第1次 | 第2次 | 第3次 | |
| 加入硫酸溶液的质量/g | 10 | 10 | 10 |
| 过滤后溶液的质量/g | 105 | 105 | 111.7 |
(1)该实验过程中产生沉淀的总质量为23.3g.
(2)该BaCl2溶液中溶质的质量分数(写出计算过程)
20.下列说法正确的是( )
| A. | 化学反应前后分子的总数可能会发生变化 | |
| B. | 燃烧都伴随着发光、放热,所以有发光、放热现象的一定是燃烧 | |
| C. | 化合物至少由两种元素组成,所以由两种元素组成的物质一定是化合物 | |
| D. | 用水灭火的原理是降低了可燃物的着火点 |
1.下列是某反应的模拟微观示意图,“ ”“
”“ ”和“
”和“ ”分别表示不同的原子,反应后方框内生成的微粒及该示意图表示的基本反应类型是 ( )
”分别表示不同的原子,反应后方框内生成的微粒及该示意图表示的基本反应类型是 ( )

 ”“
”“ ”和“
”和“ ”分别表示不同的原子,反应后方框内生成的微粒及该示意图表示的基本反应类型是 ( )
”分别表示不同的原子,反应后方框内生成的微粒及该示意图表示的基本反应类型是 ( )
| A. |  化合反应 化合反应 | B. |  复分解反应 复分解反应 | C. |  分解反应 分解反应 | D. |  置换反应 置换反应 |