题目内容
2.现有氢气、氧气、碳、铁、氧化铜、硝酸银溶液、硝酸铜溶液、稀盐酸等八种物质,请选择适当的物质完成下列化学方程式(每种物质不能重复使用).(1)有水生成的化合反应2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(2)有白色沉淀生成的复分解反应HCl+AgNO3═HNO3+AgCl↓;
(3)高温下两种黑色固体的置换反应C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
(4)生成硝酸亚铁的反应Fe+Cu(NO3)2═Fe(NO3)2+Cu.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可;要注意每种物质不能重复使用.
解答 解:(1)氢气在氧气中燃烧生成水,是有水生成的化合反应,反应的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(2)硝酸银溶液与稀盐酸反应生成氯化银沉淀和硝酸,是有白色沉淀生成的复分解反应,反应的化学方程式为:HCl+AgNO3═HNO3+AgCl↓.
(3)碳与氧化铜在高温条件下生成铜和二氧化碳,是高温下两种黑色固体的置换反应,反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(4)铁与硝酸铜溶液反应生成硝酸亚铁溶液和铜,反应的化学方程式为:Fe+Cu(NO3)2═Fe(NO3)2+Cu.
故答案为:(1)2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;(2)HCl+AgNO3═HNO3+AgCl↓;(3)C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;(4)Fe+Cu(NO3)2═Fe(NO3)2+Cu.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
12.下列关于水的叙述,不正确的是( )
| A. | 自来水属于混合物 | |
| B. | 生活中可以用过滤的方法降低水的硬度 | |
| C. | 净水常用的方法有沉淀、过滤、吸附和蒸馏等 | |
| D. | 地球上的总储水量虽然大,但是可利用的淡水资源有限 |
13.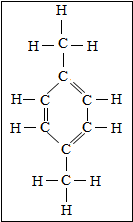 今年4月清华大学化工系学生集体捍卫PX词条事件,让更多人走进了化学、了解化学.PX的结构式如下所示,中文名称为对二甲苯(para-xylene),属于低毒类化学物质,可燃,有刺激性气味,是一种重要的化工原料.以下对PX的说法错误的是( )
今年4月清华大学化工系学生集体捍卫PX词条事件,让更多人走进了化学、了解化学.PX的结构式如下所示,中文名称为对二甲苯(para-xylene),属于低毒类化学物质,可燃,有刺激性气味,是一种重要的化工原料.以下对PX的说法错误的是( )
 今年4月清华大学化工系学生集体捍卫PX词条事件,让更多人走进了化学、了解化学.PX的结构式如下所示,中文名称为对二甲苯(para-xylene),属于低毒类化学物质,可燃,有刺激性气味,是一种重要的化工原料.以下对PX的说法错误的是( )
今年4月清华大学化工系学生集体捍卫PX词条事件,让更多人走进了化学、了解化学.PX的结构式如下所示,中文名称为对二甲苯(para-xylene),属于低毒类化学物质,可燃,有刺激性气味,是一种重要的化工原料.以下对PX的说法错误的是( )| A. | PX的相对分子质量为106g | B. | PX充分燃烧后只生成CO2和 H2O | ||
| C. | PX是低毒类有机化合物 | D. | PX的化学式为C8H10 |
11.下列各组物质分别加入到足量的水中,最终能得到无色、透明溶液的是( )
| A. | NaOH NaCl KNO3 MgCl2 | B. | NaOH Na2CO3 NaCl H2SO4 | ||
| C. | NaCl Na2SO4 AgNO3 HNO3 | D. | FeSO4 NaNO3 KCl HCl |

 .
. 自然界中碳循环问题已成为全球关注的焦点.
自然界中碳循环问题已成为全球关注的焦点.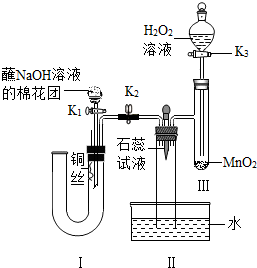 某硫酸化工厂附近居民反映:近来空气中有异味,庄稼枯黄,某学习小组对该厂附近的雨水进行检测,测得pH约为5.1,说明该区域的雨水呈酸性(填“酸性”或“碱性”或“中性”)
某硫酸化工厂附近居民反映:近来空气中有异味,庄稼枯黄,某学习小组对该厂附近的雨水进行检测,测得pH约为5.1,说明该区域的雨水呈酸性(填“酸性”或“碱性”或“中性”) 某晶牌变色眼镜的镜片在强光下会变成暗棕色,当光线变暗时,镜片几乎变成无色透明.原来,变色眼镜是在普通镜片中加入了适量的溴化银和氧化铜的微晶粒.
某晶牌变色眼镜的镜片在强光下会变成暗棕色,当光线变暗时,镜片几乎变成无色透明.原来,变色眼镜是在普通镜片中加入了适量的溴化银和氧化铜的微晶粒.