题目内容
9. 某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.
某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液可以使酚酞试液变红,是因为碱在水中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使
酚酞试液变红呢?他们设计了如图三个实验,请你和他们一起探究并完成下列问题:
(1)实验Ⅰ是为了探究Na+是否能使酚酞试液变红;
(2)实验Ⅱ加入蒸馏水的目的是探究水分子是否能使酚酞试液变红,
小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是酚酞试液中就有水分子(或氯化钠溶液中含有水分子);
(3)实验Ⅲ滴入K2CO3溶液,振荡,酚酞试液变红,向变红后的溶液中再逐滴滴入过量的CaCl2溶液,
红色逐渐消失,同时还观察到生成白色沉淀.由实验Ⅰ、Ⅱ、Ⅲ得出结论:CO32-可以使酚酞试液变红;
(4)小组同学在与老师交流上述结论时,老师说:“其实Na2CO3溶液能使酚酞试液变红也是由于溶液中存
在OH-”.你认为Na2CO3溶液中存在OH-的原因是CO32-与H2O发生反应产生OH-.
分析 (1)氯化钠中含有钠离子,可以探究钠离子能否使酚酞变色;
(2)氯化钠溶液中含有大量水分子,所以实验Ⅱ没有必要做;
(3)主要从碳酸钠溶液和氯化钙溶液的反应可以得出,碳酸根离子减少,使红色逐渐消失;
(4)氢氧根离子能够使酚酞变红,所以可以判断在碳酸钠溶液中存在氢氧根离子.
解答 解:(1)向氯化钠溶液中加酚酞不变色,说明氯化钠溶液中的粒子都不能使酚酞变红;
(2)实验Ⅱ加入蒸馏水的目的是探究水分子是否能使酚酞试液变红;氯化钠溶液中含有大量水分子,在实验Ⅰ中得到验证,所以实验Ⅱ的探究是多余的;
(3)碳酸钠溶液和氯化钙溶液反应生成碳酸钙沉淀,所以现象为产生了白色沉淀;
(4)我们知道只有氢氧根离子才能使酚酞变红,所以由碳酸钠溶液能使酚酞溶液变红,可以判断溶液中存在氢氧根离子.
故答案为:(1)探究Na+是否能使酚酞试液变红;
(2)探究水分子是否能使酚酞试液变红;酚酞试液中就有水分子(或氯化钠溶液中含有水分子);
(3)白色沉淀; Na2CO3+CaCl2═CaCO3↓+2NaCl;
(4)CO32-与H2O发生反应产生OH- (合理即可).
点评 本题考查了学生对所提供信息进行处理和利用微粒性质的差异进行实验设计的能力,要求较高.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
19.以下是我们温州的部分文化遗产,其制作过程主要属于化学变化的是( )
| A. | 温州剪纸 | B. | 平阳木偶雕刻 | C. | 泰顺米酒 | D. | 乐清黄杨木雕 |
20.下列物质的性质中属于化学性质的是( )
| A. | 胆矾是蓝色晶体 | B. | 硫酸能与铁锈反应 | ||
| C. | 硫酸钾易溶于水 | D. | 二氧化硫有刺激性气味 |
1.小明同学为探究“Na2CO3溶液与稀盐酸反应是放热反应还是吸热反应”,设计并进行了3次重复实验,结果如下表:
请你帮助填写相关内容:
(1)写出该实验涉及的化学反应方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)该实验中所用的仪器除烧杯、量筒、玻璃棒、保温瓶外,还必须用到的一种仪器是:温度计
(3)由上表数据可知:Na2CO3溶液与稀盐酸的反应是放热(选填:“放热“或“吸热“)
| 试剂1 | 试剂2 | 混合前温度/℃ | 混合后温度/℃ | |
| 35毫升稀盐酸 | 25毫升Na2CO3溶液 | 20.0 | 第1次 | 24.2 |
| 第2次 | 24.0 | |||
| 第3次 | 24.4 | |||
(1)写出该实验涉及的化学反应方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)该实验中所用的仪器除烧杯、量筒、玻璃棒、保温瓶外,还必须用到的一种仪器是:温度计
(3)由上表数据可知:Na2CO3溶液与稀盐酸的反应是放热(选填:“放热“或“吸热“)
18.实验室用加热分解方法制取氧气,并用排水法收集时有如下操作:
①向试管内装入药品
②塞好橡皮塞把试管固定在铁架台铁夹上
③连接仪器并检查装置的气密性
④给大试管加热
⑤用排水法收集氧气
⑥熄灭酒精
⑦把导管移出水面,
其正确的操作顺序是( )
①向试管内装入药品
②塞好橡皮塞把试管固定在铁架台铁夹上
③连接仪器并检查装置的气密性
④给大试管加热
⑤用排水法收集氧气
⑥熄灭酒精
⑦把导管移出水面,
其正确的操作顺序是( )
| A. | ①②③④⑤⑥⑦ | B. | ③①②④⑤⑦⑥ | C. | ③①②④⑤⑥⑦ | D. | ①③②④⑤⑦⑥ |
3.发现元素周期律的科学家是( )
| A. | 爱因斯坦 | B. | 门捷列夫 | C. | 道尔顿 | D. | 阿佛加德罗 |





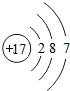 ,该元素的原子在化学反应中比较容易得到(填“得到”或“失去”)电子变成阴(填“阴”或“阳”)离子,形成的离子符号为Cl-.
,该元素的原子在化学反应中比较容易得到(填“得到”或“失去”)电子变成阴(填“阴”或“阳”)离子,形成的离子符号为Cl-.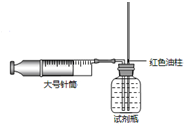 小李学习了二氧化碳知识后,进行了二氧化碳气体在水中溶解性的探究,其实验步骤及装置如下.
小李学习了二氧化碳知识后,进行了二氧化碳气体在水中溶解性的探究,其实验步骤及装置如下.