题目内容
14. “食品蒸汽加热器”常用于野外加热食物.加热袋中的固体粉末含镁粉、铁粉和氯化钠,使用时向其中加入水袋中的水,即可产生大量热.实验小组针对放热过程中的反应原理展开探究.
“食品蒸汽加热器”常用于野外加热食物.加热袋中的固体粉末含镁粉、铁粉和氯化钠,使用时向其中加入水袋中的水,即可产生大量热.实验小组针对放热过程中的反应原理展开探究.【查阅资料】
①常温下镁粉能与水反应放热而铁粉不能.
②氢氧化镁是难溶于水的白色固体.
【进行实验】
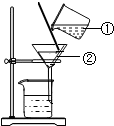
同学们用右图所示装置进行模拟实验:分别取不同成分的固体粉末放入甲中,通过分液漏斗向其中均加入8mL水,读取甲中所得固液混合物的最高温度,实验记录如下表:(实验时的室温为22.7℃;除B外,其余实验中镁粉的质量均为1.0g)
| 实验序号 | A | B | C | D | E | F |
| 固体成分 | Mg | Fe | Mg+Fe | Mg+NaCl | Fe+NaCl | Mg+Fe+NaCl |
| 乙中现象 | 少量肥皂泡,难以点燃 | ① | 少量肥皂泡,难以点燃 | 较多肥皂泡,点燃有爆鸣声 | 无肥皂泡 | 大量肥皂泡, 点燃有爆鸣声 |
| 混合物温度 | 23.1℃ | 22.8℃ | 23.1℃ | 24.2℃ | 22.8℃ | 27.2℃ |
【获得结论】
(1)实验A证明了镁粉与水能反应,反应的化学方程式为Mg+2H2O═Mg (OH)2+H2↑.
(2)使镁粉与水迅速反应并放热的最佳方法是向镁粉中加入Fe和NaCl.
【反思改进】
(1)同学们分析实验数据发现,升高的温度不足以加热食物,其可能的原因是固体药品用量少
(2)同学们根据实验结果进一步猜测,实验F中的反应结束后,甲中的固液混合物中仍然含有NaCl和铁粉,通过补充实验证明了上述猜测.补充的实验方案是:过滤,向滤渣中加入足量稀盐酸,固体溶解,有气泡冒出,溶液变浅绿色,证明有Fe,取少量固液混合物,过滤,取滤液蒸发结晶,得到白色固体(经检验为NaCl).
分析 【进行试验】①根据铁不会与水反应进行分析;
【获得结论】(1)根据水和镁反应会生成氢氧化镁和氢气进行分析;
(2)根据表中的数据进行分析;
【反思改进】(1)根据固体较少、配比不合适等原因都会造成温度上升不明显进行分析;
(2)根据铁会与盐酸反应生成氯化亚铁和氢气,氯化钠的溶解度受温度影响变化不明显进行分析.
解答 解:【进行试验】①铁不会与水反应,所以铁和水反应时,无肥皂泡产生;
【获得结论】(1)水和镁反应会生成氢氧化镁和氢气,化学方程式为:Mg+2H2O═Mg (OH)2+H2↑;
(2)通过分析表中各物质之间的反应和升高的温度可知,使镁粉与水迅速反应并放热的最佳方法是向镁粉中加入Fe和NaCl;
【反思改进】(1)固体较少、配比不合适等原因都会造成温度上升不明显,所以分析实验数据发现,升高的温度不足以加热食物,其可能的原因是:固体药品用量少;
(2)铁会与盐酸反应生成氯化亚铁和氢气,氯化钠的溶解度受温度影响变化不明显,所以补充的实验方案是:取少量固液混合物,过滤,向滤渣中加入足量稀盐酸,固体溶解,有气泡冒出,溶液变浅绿色,证明有Fe,取少量固液混合物,经过过滤,取滤液蒸发结晶,得到白色固体(经检验为NaCl).
故答案为:【进行试验】①无肥皂泡;
【获得结论】(1)Mg (OH)2+H2↑;
(2)Fe和NaCl;
【反思改进】(1)固体药品用量少;
(2)过滤,向滤渣中加入足量稀盐酸,固体溶解,有气泡冒出,溶液变浅绿色,证明有Fe;取滤液蒸发结晶.
点评 本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.

(一)气体的制取和收集
现有如图所示的实验装置:

(1)A装置可用于制氢气、氧气、二氧化碳气体,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑、2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2O+O2↑、CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)实验室需少量甲烷气,可用加热无水醋酸钠与碱石灰的固体混合物制得.制甲烷气的发生装置应选用B(填字母)装置;收集甲烷气可选用C或E装置,由此推断甲烷气具有的物理性质是不溶于水,密度比空气小.
(3)实验室用A装置制取气体前,先向长颈漏斗中加水淹没长颈漏斗的下端,其目的是为了防止气体从长颈漏斗逸出.
(4)用B、D组合制取制氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,检验氧气已集满的方法是带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了.
(二)某食品包装袋中有一个小纸袋,上面写“生石灰干燥剂,请勿食用”.该食品已放置两月有余.请你对下列问题进行探究.
(1)小纸袋中的物质能否继续作干燥剂?
| 实验步骤 | 实验现象 | 结论 |
| 取足量的小纸袋中的固体放入 烧杯中,加入适量的水,触摸杯壁 | 杯壁变热 | 可继续作干燥剂 |
(3)请设计实验证明(2)中你所填的物质是否存在加入足量的盐酸,观察是否产生气泡.
| A. | 吸附性 | B. | 还原性 | C. | 稳定性 | D. | 可燃性 |
| A. | 等质量的CO和CO2,CO和CO2中氧元素的质量比为11:14 | |
| B. | 等质量的Al和Mg分别与足量稀硫酸充分反应,生成H2的质量相等 | |
| C. | 等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量不相等 | |
| D. | 等质量的质量分数均为4%氢氧化钠溶液与稀盐酸充分反应,所得溶液显中性 |
| A. | ④③①②⑤ | B. | ②①④③⑤ | C. | ②④①③⑤ | D. | ④①②③⑤ |