题目内容
6. 如图是一盏废旧台灯,某实验小组的同学利用它进行观察分析并完成相关实验.
如图是一盏废旧台灯,某实验小组的同学利用它进行观察分析并完成相关实验.(1)小明发现台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的氧气和水等发生了化学反应.
(2)小红发现铝箔反光片呈银白色,无锈迹,原因是铝表面有一层致密的氧化膜,生成该氧化膜的化学方程式为4Al+3O2═2Al2O3.
分析 (1)铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果.
(2)铝表面有一层致密的氧化膜,是因为铝在常温下能与氧气反应生成氧化铝,写出反应的化学方程式即可.
解答 解:(1)小明发现台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的氧气和水等发生了化学反应.
(2)铝表面有一层致密的氧化膜,是因为铝在常温下能与氧气反应生成氧化铝,反应的化学方程式为:4Al+3O2═2Al2O3.
故答案为:(1)氧气和水;(2)4Al+3O2═2Al2O3.
点评 本题难度不大,掌握铁锈蚀的条件(铁与氧气、水同时接触)、金属铝的抗腐蚀性(常温下与氧气反应生成氧化铝)是正确解答本题的关键.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
16.根据如图装置图回答问题.
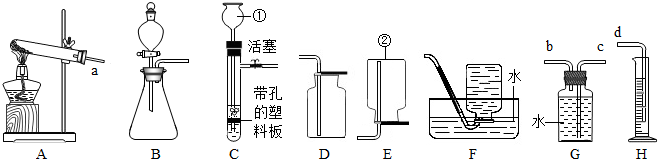
(1)实验室用一定质量的氯酸钾制取氧气,通过排水量测定所收集到的氧气体积.
①写出该反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
②各装置的连接顺序是:abcd.(用管口字母表示)
(2)某化学探究小组用HCl与大理石反应研究影响反应剧烈程度的因素.实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10g;所用HCl的质量分数为9.125%、18.25%,每次实验HCl的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1g/cm3;大理石中杂质不与盐酸反应).
【提出问题】:影响HCl与大理石反应的剧烈程度的因素有哪些?
【做出猜想】:
猜想一:大理石规格;猜想二:所用HCl溶液的质量分数;猜想三:实验温度.
【实验设计与实施】:完成以下实验设计方案并实验.
【实验结论】:在其他条件不变时,盐酸溶液质量分数越大,反应越剧烈;温度越高,反应越剧烈;固体的颗粒越小,反应越剧烈..

(1)实验室用一定质量的氯酸钾制取氧气,通过排水量测定所收集到的氧气体积.
①写出该反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
②各装置的连接顺序是:abcd.(用管口字母表示)
(2)某化学探究小组用HCl与大理石反应研究影响反应剧烈程度的因素.实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10g;所用HCl的质量分数为9.125%、18.25%,每次实验HCl的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1g/cm3;大理石中杂质不与盐酸反应).
【提出问题】:影响HCl与大理石反应的剧烈程度的因素有哪些?
【做出猜想】:
猜想一:大理石规格;猜想二:所用HCl溶液的质量分数;猜想三:实验温度.
【实验设计与实施】:完成以下实验设计方案并实验.
| 实验 编号 | T/℃ | 大理石 规格 | HCl的 质量分数 | 完全反应 的时间/s | 实验目的 |
| ① | 25 | 粗颗粒 | 18.25% | 160 | (Ⅰ)实验①和②探究同体积下HCl质量分数对该反应剧烈程度的影响. (Ⅱ)实验①和③探究温度对该反应剧烈程度的影响. (Ⅲ)实验①和④探究大理石规格对该反应剧烈程度的影响. |
| ② | 210 | ||||
| ③ | 35 | 粗颗粒 | 18.25% | 60 | |
| ④ | 100 |
17.大多数花卉喜欢微酸性土壤,某花卉长势不佳,经测定盆中土壤pH为8.2,在施用较稀FeSO4溶液浇灌后长势良好,这说明FeSO4溶液( )
| A. | 显碱性 | B. | 显酸性 | C. | 显中性 | D. | 无法判断 |
14. 钚(Pu)是一种稀土元素,该元素在周期表中的信息如图所示,下列有关说法错误的是( )
钚(Pu)是一种稀土元素,该元素在周期表中的信息如图所示,下列有关说法错误的是( )
 钚(Pu)是一种稀土元素,该元素在周期表中的信息如图所示,下列有关说法错误的是( )
钚(Pu)是一种稀土元素,该元素在周期表中的信息如图所示,下列有关说法错误的是( )| A. | 钚是金属元素 | B. | 钚原子的质子数为94 | ||
| C. | 钚元素的相对原子质量为224 | D. | 钚原子的中子数为94 |
11.某化学兴趣小组围绕“酸和碱的中和反应”学习,进行了如下实验:
实验一:取5mL氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,观察到溶液变为红色,向溶液中加入稀盐酸,用玻璃棒搅拌,溶液褪为无色,但出现了一个奇怪的现象:试管中产生气泡.
【提出问题】
产生气泡的原因是什么?
【实验分析】
小明同学发现氢氧化钠溶液没有盖紧瓶塞,由此推断,可能是氢氧化钠溶液在空气中变质2NaOH+CO2═Na2CO3+H2O(写出化学方程式)的缘故,变质后的生成物与盐酸反应后生成了CO2(些化学式)的结果.
实验二:小组同学重新配制氢氧化钠溶液,重复上述实验.观察到溶液褪至无色,该反应的化学方程式为NaOH+HCl═NaCl+H2O.
【提出问题】
对反应后溶液中的溶质进行探究.
【提出猜想】
猜想一:只有NaCl
猜想二:有NaCl和NaOH
猜想三:有NaCl和HCl
你认为猜想二不合理,其理由是此时溶液呈无色,而氢氧化钠能使酚酞试液变红.
【设计实验】
实验一:取5mL氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,观察到溶液变为红色,向溶液中加入稀盐酸,用玻璃棒搅拌,溶液褪为无色,但出现了一个奇怪的现象:试管中产生气泡.
【提出问题】
产生气泡的原因是什么?
【实验分析】
小明同学发现氢氧化钠溶液没有盖紧瓶塞,由此推断,可能是氢氧化钠溶液在空气中变质2NaOH+CO2═Na2CO3+H2O(写出化学方程式)的缘故,变质后的生成物与盐酸反应后生成了CO2(些化学式)的结果.
实验二:小组同学重新配制氢氧化钠溶液,重复上述实验.观察到溶液褪至无色,该反应的化学方程式为NaOH+HCl═NaCl+H2O.
【提出问题】
对反应后溶液中的溶质进行探究.
【提出猜想】
猜想一:只有NaCl
猜想二:有NaCl和NaOH
猜想三:有NaCl和HCl
你认为猜想二不合理,其理由是此时溶液呈无色,而氢氧化钠能使酚酞试液变红.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入石蕊试液(锌粒) | 溶液变红(产生气泡) | 猜想三成立 |
18.下列说法错误的是( )
| A. | 原子是由原子核和电子构成 | B. | 原子是化学变化中的最小粒子 | ||
| C. | 分子是保持物质性质的最小粒子 | D. | 只含一种元素的物质可能是混合物 |
5.化学反应前后,生成物的总质量与反应物的总质量相等是因为( )
| A. | 反应前后物质的种类没有变 | |
| B. | 反应前后原子的种类和数目没有变化 | |
| C. | 反应前后分子的种类和数目没有变化 | |
| D. | 反应前后元素的种类没有变化 |