题目内容
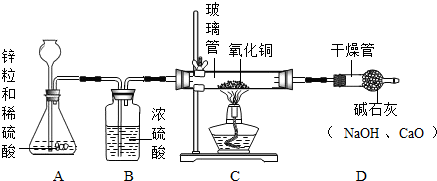
11.某化学兴趣小组围绕“酸和碱的中和反应”学习,进行了如下实验:实验一:取5mL氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,观察到溶液变为红色,向溶液中加入稀盐酸,用玻璃棒搅拌,溶液褪为无色,但出现了一个奇怪的现象:试管中产生气泡.
【提出问题】
产生气泡的原因是什么?
【实验分析】
小明同学发现氢氧化钠溶液没有盖紧瓶塞,由此推断,可能是氢氧化钠溶液在空气中变质2NaOH+CO2═Na2CO3+H2O(写出化学方程式)的缘故,变质后的生成物与盐酸反应后生成了CO2(些化学式)的结果.
实验二:小组同学重新配制氢氧化钠溶液,重复上述实验.观察到溶液褪至无色,该反应的化学方程式为NaOH+HCl═NaCl+H2O.
【提出问题】
对反应后溶液中的溶质进行探究.
【提出猜想】
猜想一:只有NaCl
猜想二:有NaCl和NaOH
猜想三:有NaCl和HCl
你认为猜想二不合理,其理由是此时溶液呈无色,而氢氧化钠能使酚酞试液变红.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入石蕊试液(锌粒) | 溶液变红(产生气泡) | 猜想三成立 |
分析 实验一:根据物质的性质进行分析,氢氧化钠能与盐酸反应生成氯化钠和水,酚酞在酸性和中性溶液中为无色,在碱性溶液中为红色;考虑氢氧化钠与二氧化碳反应生成碳酸钠和水等;
实验二:跟据已有的知识进行分析,氢氧化钠溶液呈碱性,能使酚酞试液变红,能与盐酸反应生成氯化钠和水;盐酸能使紫色石蕊试液变红,酸碱能发生中和反应,据此解答.
解答 解:实验一:取5mL氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,观察到溶液变为红色;氢氧化钠与二氧化碳反应生成碳酸钠和水.该反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O.碳酸钠与稀盐酸发生复分解反应,生成氯化钠、二氧化碳气体和水,其化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑,故产生气泡的原因是变质后的生成物与盐酸反应后生成了二氧化碳;
实验二:小组同学重新配制氢氧化钠溶液,重复上述实验.观察到溶液褪至无色,该反应的化学方程式为NaOH+HCl═NaCl+H2O;
由于氢氧化钠呈碱性,能使酚酞试液变红,而此时溶液是无色的,故一定不会有氢氧化钠剩余,故填:二,此时溶液呈无色,而氢氧化钠能使酚酞试液变红;
设计实验:猜想三中含有盐酸,要证明盐酸的存在,可以加入石蕊试液,盐酸能使石蕊试液变红,故填:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入石蕊试液(锌粒) | 溶液变红(产生气泡) | 猜想三成立 |
实验一:红.【实验分析】2NaOH+CO2═Na2CO3+H2O,CO2.
实验二:NaOH+HCl═NaCl+H2O.
【提出猜想】二,此时溶液呈无色,而氢氧化钠能使酚酞试液变红.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 石蕊试液(锌粒) | 溶液变红(产生气泡) | 猜想三成立 |
点评 本题考查了常见酸与碱之间的反应以及应用,还考查了氢氧化钠的变质等,可以依据酸、碱的性质进行.

练习册系列答案
相关题目
1.比较推理是化学学习中常用的思维方法,下列有关物质的比较推理中正确的是( )
| A. | 同一化合物中,金属一定显正价,则非金属一定显负价 | |
| B. | 二氧化碳会造成“温室效应”,所以二氧化碳是一种大气污染物 | |
| C. | 水和过氧化氢的组成元素相同,所以两者化学性质相同 | |
| D. | 两种物质相互反应生成盐和水,则该反应不一定是中和反应 |
5. 家庭生火经长从“大木块”到“小木块”的变化,其目的是( )
家庭生火经长从“大木块”到“小木块”的变化,其目的是( )
 家庭生火经长从“大木块”到“小木块”的变化,其目的是( )
家庭生火经长从“大木块”到“小木块”的变化,其目的是( )| A. | 增大可燃物的热值 | B. | 提高可燃物的着火点 | ||
| C. | 增大可燃物与空气的接触面积 | D. | 提高空气中氧气的含量 |
6.在珍珠中加入稀盐酸有气泡产生,且生成的气体能使澄清石灰水变浑浊,则珍珠中可能含有的离子是( )
| A. | 氯离子 | B. | 碳酸根离子 | C. | 铵根离子 | D. | 氢氧根离子 |
 如图是一盏废旧台灯,某实验小组的同学利用它进行观察分析并完成相关实验.
如图是一盏废旧台灯,某实验小组的同学利用它进行观察分析并完成相关实验.