题目内容
17. 冬季市场上热销一种叫“暖宝宝”取暖贴.取暖贴的持续放热可以促进人体微循环,恢复正常的生理机能,从而消除疼痛,治疗疾病.对关节炎、肩周炎、腰腿痛等病痛都有很好的效果的.图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
冬季市场上热销一种叫“暖宝宝”取暖贴.取暖贴的持续放热可以促进人体微循环,恢复正常的生理机能,从而消除疼痛,治疗疾病.对关节炎、肩周炎、腰腿痛等病痛都有很好的效果的.图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.(1)发热剂需接触到空气才会发热,原因是铁要与水、氧气等物质共同作用才会生锈.
(2)发热剂成分中氯化钠的作用是加速铁粉生锈,更快地放出热量.
(3)铁生锈放热是利用化学能转化为内能(写出能量转化)
分析 (1)铁与水和氧气同时接触时容易生锈;
(2)如果有盐溶液存在时,会使生锈速度加快;
(3)铁生锈发生了化学变化.
解答 解:(1)铁与水单独接触,或单独与氧气接触,都不容易生锈,只有与水和氧气同时接触时才容易生锈;发热剂需要接触到空气才会发热,原因是铁要与水、氧气等共同作用才会生锈.故填:水、氧气;
(2)当有盐溶液存在时,生锈的速度加快,所以发热剂成分中有氯化钠;故填:加速铁粉生锈,更快地放出热量;
(3)铁生锈发生了化学变化,放出热量,属于化学能转化为内能.故填:化学能转化为内能.
点评 本题考查铁生锈的条件及利用铁生锈原理取暖,应用到了生活中.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
8. 人们在装修时,经常开窗通风,目的是排除装修材料释放出的有毒气体甲醛,其分子的模型如图所示,据此下列叙述正确的是( )
人们在装修时,经常开窗通风,目的是排除装修材料释放出的有毒气体甲醛,其分子的模型如图所示,据此下列叙述正确的是( )
 人们在装修时,经常开窗通风,目的是排除装修材料释放出的有毒气体甲醛,其分子的模型如图所示,据此下列叙述正确的是( )
人们在装修时,经常开窗通风,目的是排除装修材料释放出的有毒气体甲醛,其分子的模型如图所示,据此下列叙述正确的是( )| A. | 甲醛由碳、氢、氮三种元素组成 | |
| B. | 甲醛分子是由1个碳原子、1个氧原子和2个氢原子构成 | |
| C. | 甲醛中C、H、O三种元素的个数比是1:2:1 | |
| D. | 甲醛是由多原子分子构成的有机小分子化合物 |
5.植物色素包括吐绿素和花青素等.资料表明:①绿色植物能进行光合作用,其中叶绿素(C55H72O5N4Mg)功不可没,植物光合作用合成的淀粉只有转化成葡萄糖(能使植物细胞液呈酸性),才能输送到植物的各部分去.②花青素随溶液pH的变化呈现的颜色如表:
根据以上材料,请回答以下问题:
(1)叶绿素中氢、氧元素的质量比为9:10.
(2)花青素在稀盐酸中呈现的颜色可能为红色或粉红色.
| 溶液pH | 2 | 4 | 10 | 12 |
| 颜色 | 红 | 粉红 | 蓝 | 深蓝 |
(1)叶绿素中氢、氧元素的质量比为9:10.
(2)花青素在稀盐酸中呈现的颜色可能为红色或粉红色.
12.下列类推正确的是( )
| A. | 质子数相同的一类原子总称为元素,则钠原子和钠离子的质子数相同 | |
| B. | 单质是一种元素组成的,所以有一种元素组成的物质就是单质 | |
| C. | 分子是由原子构成的,所以分子的质量和体积一定比原子大 | |
| D. | 氧化物都含有氧元素,所以含氧元素的化合物一定都是氧化物 |
2.推理是一种重要的思维方法,以下推理合理的是( )
| A. | 碱性溶液的pH都大于7,所以碱溶液pH一定大于7 | |
| B. | 铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀 | |
| C. | 因为H2O和H2O2的组成元素相同,所以两者的化学性质相同 | |
| D. | 因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 |
6.FeCl3溶液腐蚀铜、铁的反应分别为:Cu+2FeCl3=2FeCl2+CuCl2、Fe+2FeCl3=3FeCl2.从腐蚀过镀铜器件的废液中回收铜,并重新制得FeCl3的流程如下:
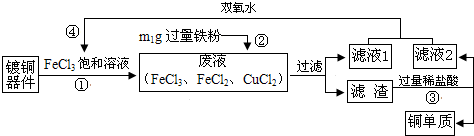
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 步骤②中发生化合反应与置换反应 | |
| B. | “滤液1”中一定含FeCl2,一定不含CuCl2 | |
| C. | 步骤④反应为:2M+2FeCl2+H2O2=2FeCl3+2H2O,M是HCl | |
| D. | 由于部分Cu与FeCl3发生反应造成回收的铜单质比废液中的铜元素质量变少了 |
3.下列所示的图象与实验相符合的是( )
| A. |  饱和Ca(OH)2溶液升温 | |
| B. |  镁在空气中燃烧 | |
| C. |  向含少量氢氧化钠的碳酸钠溶液中逐滴加入稀盐酸至过量 | |
| D. |  等质量的镁片、锌片分别和足量的稀硫酸反应 |
 1673年,英国化学家波义耳曾经做了这样一个实验:在一个敞口的容器中加热金属汞(汞在加热的条件下能与氧气反应生成红色固体氧化汞),结果发现反应后的容器中物质的质量增加了.现某课题小组成员通过测定氧化汞分解前后反应物和生成物的质量是否相等来验证质量守恒定律.(已知:标准状况下氧气的密度为ρ,氧化汞分解的反应方程式:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑)
1673年,英国化学家波义耳曾经做了这样一个实验:在一个敞口的容器中加热金属汞(汞在加热的条件下能与氧气反应生成红色固体氧化汞),结果发现反应后的容器中物质的质量增加了.现某课题小组成员通过测定氧化汞分解前后反应物和生成物的质量是否相等来验证质量守恒定律.(已知:标准状况下氧气的密度为ρ,氧化汞分解的反应方程式:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑)