题目内容
6.FeCl3溶液腐蚀铜、铁的反应分别为:Cu+2FeCl3=2FeCl2+CuCl2、Fe+2FeCl3=3FeCl2.从腐蚀过镀铜器件的废液中回收铜,并重新制得FeCl3的流程如下: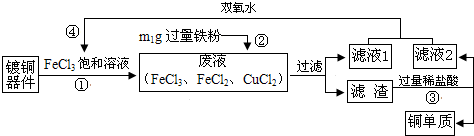
下列说法不正确的是( )
| A. | 步骤②中发生化合反应与置换反应 | |
| B. | “滤液1”中一定含FeCl2,一定不含CuCl2 | |
| C. | 步骤④反应为:2M+2FeCl2+H2O2=2FeCl3+2H2O,M是HCl | |
| D. | 由于部分Cu与FeCl3发生反应造成回收的铜单质比废液中的铜元素质量变少了 |
分析 腐蚀废液中含有氯化铜、氯化亚铁以及氯化铁,铁可以置换金属铜,可以和三价铁反应,铜不能盐酸反应,而金属铁可以,氯气具有氧化性,能将亚铁离子氧化为三价铁.据此解答.
解答 解:A、根据图框,②发生反应为:Fe+2FeCl3=3FeCl2、Fe+CuCl2=Cu+FeCl2;故步骤②中发生化合反应与置换反应,说法正确;
B、因为步骤②中加入了过量的铁粉,则一定在“滤液1”中不会含CuCl2;故说法正确;
C、由图可知,步骤④反应为:2M+2FeCl2+H2O2=2FeCl3+2H2O,由质量守恒定律科推出M是HCl,说法正确;
D、由题意可知,虽然部分Cu与FeCl3发生反应,但生成的氯化铜又与过量的铁发生了反应,废液中不含有铜元素,故说法错误.
故选:D.
点评 本题考查学生铁及化合物的性质,可以根据所学知识结合金属活动性顺序及题目信息进行回答,难度较大.

练习册系列答案
相关题目
14.向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤.
$\stackrel{25℃}{100g水}$$→_{37.2g}^{加入A}$①$→_{4.2g}^{加入A}$②$→_{至60℃}^{升温}$③$→_{9g}^{加入A}$④$→_{至50℃}^{降温}$⑤
表为A在不同温度下的溶解度,则在编号为①~⑤的溶液中(下列小题均填序号):
(1)属于饱和溶液的是溶液②⑤.
(2)溶质质量分数最大是溶液④⑤.
(3)溶质质量分数相等是溶液④⑤.
(4)溶液中没有固体存在的是①、③、④、⑤.
$\stackrel{25℃}{100g水}$$→_{37.2g}^{加入A}$①$→_{4.2g}^{加入A}$②$→_{至60℃}^{升温}$③$→_{9g}^{加入A}$④$→_{至50℃}^{降温}$⑤
表为A在不同温度下的溶解度,则在编号为①~⑤的溶液中(下列小题均填序号):
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
(2)溶质质量分数最大是溶液④⑤.
(3)溶质质量分数相等是溶液④⑤.
(4)溶液中没有固体存在的是①、③、④、⑤.
1.下列日常生活中的变化,属于物理变化的一组是( )
| A. | 工业分离液态空气制氧气 | B. | 菜刀生锈 | ||
| C. | 火药爆炸 | D. | 煤的干馏 |
11.实验室有一瓶无色溶液,标签已模糊,为探究该溶液中的溶质究竟是什么物质,某兴趣小组的同学进行了一系列实验:
(1)小张同学先取该无色溶液少许,滴入紫色石蕊试液,石蕊试液变红,此时可得出的结论是该溶液呈酸性.
(2)小王同学发现尽管试剂瓶标签已模糊,但依稀可见SO4字样.于是,他设计了甲、乙两个方案,并分别取样品实验、记录相关现象.

上述方案中,能确定该无色溶液中含有硫酸根的方案是方案甲、方案乙;
方案乙中,加入足量稀HCl的作用是排除碳酸根离子和银离子的干扰.
(3)同学们发现标签上还有20.0%的字样,老师告诉他们,这瓶试剂是硫酸、硫酸钠、硫酸镁溶液中的一种.同学通过查阅资料得知,常温下这三种物质的溶解度如表:
根据上述信息,同学们分析后认为此溶液一定不是Na2SO4Na2SO4溶液,原因是常温下硫酸钠溶液的最大质量分数是17%,不能配置出20%的溶液.
(1)小张同学先取该无色溶液少许,滴入紫色石蕊试液,石蕊试液变红,此时可得出的结论是该溶液呈酸性.
(2)小王同学发现尽管试剂瓶标签已模糊,但依稀可见SO4字样.于是,他设计了甲、乙两个方案,并分别取样品实验、记录相关现象.

上述方案中,能确定该无色溶液中含有硫酸根的方案是方案甲、方案乙;
方案乙中,加入足量稀HCl的作用是排除碳酸根离子和银离子的干扰.
(3)同学们发现标签上还有20.0%的字样,老师告诉他们,这瓶试剂是硫酸、硫酸钠、硫酸镁溶液中的一种.同学通过查阅资料得知,常温下这三种物质的溶解度如表:
| 物质 | H2SO4 | Na2SO4 | MgSO4 |
| 溶解度/g | 与水任意比互溶 | 19.0 | 39.0 |
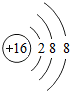 表示的是S2-(填离子符号).
表示的是S2-(填离子符号). 冬季市场上热销一种叫“暖宝宝”取暖贴.取暖贴的持续放热可以促进人体微循环,恢复正常的生理机能,从而消除疼痛,治疗疾病.对关节炎、肩周炎、腰腿痛等病痛都有很好的效果的.图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
冬季市场上热销一种叫“暖宝宝”取暖贴.取暖贴的持续放热可以促进人体微循环,恢复正常的生理机能,从而消除疼痛,治疗疾病.对关节炎、肩周炎、腰腿痛等病痛都有很好的效果的.图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热. 如图为某制药厂生产的高钙片标签上的部分说明,请仔细阅读后回答下列问题.
如图为某制药厂生产的高钙片标签上的部分说明,请仔细阅读后回答下列问题.