题目内容
7.某金属A的氯化物溶液200g,溶质质量分数为11.10%向其中加入AgNO3溶液至不再产生沉淀为止,过滤干燥得沉淀的质量为57.4g.该金属的相对原子质最为40,氯化物的化学式为CaCl2.分析 根据题目中关于物质质量的关系,结合具体的反应可利用所学的知识书写该反应的方程式,然后利用化学方程式的计算分别对A的相对原子质量进行讨论,进而判断金属的种类.
解答 解:设金属的化合价是x,原子量是y,因氯化物与硝酸银反应会生成氯化银和A的硝酸盐,则有
AClx+xAgNO3=xAgCl↓+A(NO3)x
y+35.5x 143.5x
200g×11.10% 57.4g
$\frac{y+35.5x}{143.5x}$=$\frac{200g×11.10%}{57.4g}$
5740x=287y
由于金属的化合价一般是从1到3,分别讨论可得金属的原子量分别是:化合价是1时原子量是20,为二时原子量是40,为三时原子量是60,金属的原子量是20与60时无此金属,所以有x=2;y=40
则该金属元素是钙
这种氯化物的化学式 CaCl2
故答案为:40; CaCl2
点评 此题是一道综合计算题,解题的关键是对相关计算中数据的分析,属于一道考查学生综合能力的难题.

练习册系列答案
相关题目
17.下列鉴别两种不同物质的方法中不正确的是( )
| A. | 氮气与二氧化碳-----点燃的木条 | |
| B. | 氧化钙与硝酸铵------加水,测量溶液温度的变化 | |
| C. | 尿素和硫酸铵--------加熟石灰,研磨 | |
| D. | 氧化铜与铁粉---------用磁铁吸引 |
15.下列关于溶液的说法,错误的是( )
| A. | 向饱和的硫酸铜溶液中加入一定量的硝酸钾晶体,晶体可以被溶解 | |
| B. | 擦过汤汁的抹布晒干后出现白色斑迹,是因为汤汁水分蒸发后盐分结晶析出 | |
| C. | 碘酒溶液中,溶质是碘,溶剂是酒精 | |
| D. | 氯化钠在20℃时溶解度是36g,则100g的氯化钠溶液中含有氯化钠36g |
19.下列实验过程中,相关实验操作正确的是( )
| A. |  取样 | B. |  加药品 | C. |  加热 | D. |  熄灭酒精灯 |
 红枣包装中常使用一种袋装防腐剂,品名为“504 双 吸剂”,其标签如图所示. 同学们对一包久置的“504 双吸剂”固样品 很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504 双 吸剂”,其标签如图所示. 同学们对一包久置的“504 双吸剂”固样品 很好奇,设计实验进行探究. 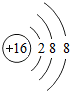 表示的是S2-(填离子符号).
表示的是S2-(填离子符号). 冬季市场上热销一种叫“暖宝宝”取暖贴.取暖贴的持续放热可以促进人体微循环,恢复正常的生理机能,从而消除疼痛,治疗疾病.对关节炎、肩周炎、腰腿痛等病痛都有很好的效果的.图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
冬季市场上热销一种叫“暖宝宝”取暖贴.取暖贴的持续放热可以促进人体微循环,恢复正常的生理机能,从而消除疼痛,治疗疾病.对关节炎、肩周炎、腰腿痛等病痛都有很好的效果的.图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.