题目内容
4. 哈尔滨第四十七中学创办于1965年,至今已建校整整50年,学校规模不断扩大.学生学习的同时,运动健康也是学校的教育主题,如图是我校新建体育馆和健身房,下列有关说法错误的是( )
哈尔滨第四十七中学创办于1965年,至今已建校整整50年,学校规模不断扩大.学生学习的同时,运动健康也是学校的教育主题,如图是我校新建体育馆和健身房,下列有关说法错误的是( )| A. | 各馆室均采用LED灯照明设备,亮度高而且节约能源 | |
| B. | 粉刷墙壁时所用的石灰浆主要成分是碳酸钙 | |
| C. | 健身房的健身车车架主要采用的锰钢属于金属材料 | |
| D. | 各馆室的使用让学生更多体会到运动的乐趣 |
分析 A、根据LED灯的优点进行解答;
B、根据粉刷墙壁时,粉刷墙壁所用石灰浆的主要成分为氢氧化钙进行解答;
C、根据锰钢是合金,属于金属材料进行解答;
D、根据建造体育馆和健身房的意义进行解答.
解答 解:
A、各馆室均采用LED灯照明设备,亮度高而且节约能源,故正确;
B、粉刷墙壁时,粉刷墙壁所用石灰浆的主要成分为氢氧化钙,而不是碳酸钙,故错误;
C、健身房的健身车车架主要采用的锰钢是铁的合金,属于金属材料,故正确;
D、各馆室的使用让学生更多体会到运动的乐趣,故正确.
故选:B.
点评 解答本题要了解材料的分类、常见污染的来源及治理污染的方法.可以结合生活常识快速判断.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案
相关题目
15.有三种金属X、Y、Z,它们与酸或碱溶液可以发生如下反应:①Y+X(NO3)2=Y(NO3)2+X②X+H2SO4=XSO4+H2↑③Z不与盐酸反应.则该三种金属的活动性顺序为( )
| A. | X>Y>Z | B. | Y>Z>X | C. | Y>X>Z | D. | Z>Y>X |
12.分析推理是化学学习中常用的思维方法,下列有关事实和推理得到的结论合理的是( )
| 事实 | 结论 | |
| A | 酸雨的pH小于7 | pH小于7的雨水一定是酸雨 |
| B | 金刚石和石墨均是由碳元素组成的单质 | 金刚石和石墨属于同一种物质 |
| C | 氢气和氧气混合点燃可能爆炸 | 点燃可燃性气体之前应先检验纯度 |
| D | Al在常温下就能与O2发生反应,Fe在常温下几乎不与O2反应 | Al的抗腐蚀性能比Fe弱 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
9.下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 工业上高炉炼铁 Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2氧化反应 | |
| B. | 农药波尔多液盛放在铁制容器中 Fe+CuSO4=FeSO4+Cu 置换反应 | |
| C. | 敞口放置的氢氧化钠固体变质:2NaOH+CO2=Na2CO3+H2O 复分解反应 | |
| D. | 高温煅烧石灰石获取生石灰和二氧化碳:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ 分解反应 |
16.为测定石灰石钙元素的质量分数,某同学取一定量该石灰石(杂质不含钙元素且不参加反应也不溶于水)研碎后直接煅烧一段时间后,称量剩余固体的质量为103g,向其加入500g质量分数为14.6%的稀盐酸恰好完全反应,过滤后称量剩余固体质量为25g,则该石灰石中钙元素的质量分数为( )
| A. | 28% | B. | 32% | C. | 40% | D. | 50% |
13.下列图示的实验操作能达到对应目的是( )
| A. | 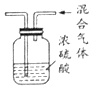 除去氧气中的水蒸气 | B. | 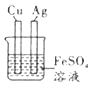 验证Fe、Cu、Ag的金属活动性强弱 | ||
| C. | 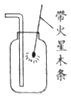 检验O2是否收集满 | D. | 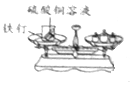 验证质量守恒定律 |
15.很多水龙头是铜质镀铬的,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,同学们进行如下探究活动:
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
【回答问题】(1)用砂纸打磨金属片的目的是除去表面的氧化物.
(2)实验一所发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是铝和铬都能够和硫酸铜反应,无法比较铬和铝的金属活动性强弱.
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是A1、CrSO4溶液、Cu.
【归纳】比较金属活动性强弱的方法有
①通过金属与酸反应快慢判断金属活动性强弱
②通过金属与盐溶液反应判断金属活动性强弱.
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮.
| 实验一 | 实验二 | 实验三 | |
| 实验 方案 |  |  |  |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 铜片无明显现象 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能和稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是铝、铬、铜 | |||
(2)实验一所发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是铝和铬都能够和硫酸铜反应,无法比较铬和铝的金属活动性强弱.
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是A1、CrSO4溶液、Cu.
【归纳】比较金属活动性强弱的方法有
①通过金属与酸反应快慢判断金属活动性强弱
②通过金属与盐溶液反应判断金属活动性强弱.
