题目内容
13.下列含氮的物质中,氮元素呈现的化合价共有( )NO、HNO2、N2、N2O、NH4NO3、N2O4.
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
分析 根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,结合各化学式进行解答本题.
解答 解:根据单质中元素的化合价为0,N2属于单质,故N2中氮元素的化合价为0.
氢元素显+1价,氧元素显-2价,设HNO2中氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×2=0,则x=+3价.
在化合物中正负化合价代数和为零,氧元素显-2价,NO、N2O、N2O4中氮元素的化合价分别显+2价、+1价、+4价.
铵根的化合价为+1价,硝酸根的化合价为-1价,在铵根中,H元素的化合价为+1价,设N元素的化合价为y,则y+(+1)×4=+1,解得y=-3,即铵根中氮元素的化合价为-3价;在硝酸根中,氧元素的化合价为-2价,设N元素的化合价为z,则z+(-2)×3=-1,解得z=+5,即硝酸根中氮元素的化合价为+5价.
综上所述,这六种物质中氮元素显示的化合价共有7种.
故选D.
点评 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
5.“对比试验”是化学学习中行之有效的思维方法,以下实验没有体现“对比”的是( )
| A. |  测定质量守恒定律 | B. |  探究微粒运动 | ||
| C. |  测定空气中氧气含量 | D. |  测定CO2的性质 |
8. 根据表中内容回答下列问题:
根据表中内容回答下列问题:
(1)随温度升高,硝酸钾溶解度的变化趋势是增大(填“增大”“减小”或“不变”);
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是20℃~40℃;
(3)取KNO3、NaCl两种固体各36g分别放入20℃时的100g水中充分溶解,20℃时有如图所示的实验现象,烧杯B中溶解的物质NaCl.
 根据表中内容回答下列问题:
根据表中内容回答下列问题:| 温度/℃ 溶解度/g | 0 | 20 | 40 | 60 | 80 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| Ca(OH)2 | 0.173 | 0.165 | 0.121 | 0.116 | 0.094 |
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是20℃~40℃;
(3)取KNO3、NaCl两种固体各36g分别放入20℃时的100g水中充分溶解,20℃时有如图所示的实验现象,烧杯B中溶解的物质NaCl.
9.下列有关物质的检验、鉴别、除杂、分离所用的试剂或方法正确的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 检验生石灰中是否含有杂质石灰石 | 水或稀盐酸 |
| B | 除去BaCl2溶液中的Ba(OH)2 | 加适量的稀硫酸后过滤 |
| C | 鉴别食盐和蔗糖 | 品尝 |
| D | 除去CO中混有的CO2 | NaOH溶液、浓H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
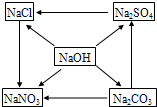 有五种化合物,它们两两之间发生的某些转化关系如图箭头所示.请回答:
有五种化合物,它们两两之间发生的某些转化关系如图箭头所示.请回答:
