题目内容
10.某化学兴趣小组的同学对蜡烛的燃烧和空气中氧气含量的测定进行了一系列的探究,请你参与并回答下列问题.
【发现问题 1】点燃蜡烛,发现蜡烛火焰的明亮程度不一样,是什么原因所致呢?
【猜想与假设1】猜想①:蜡烛中可燃物成分不一样;
猜想②:蜡烛烛心棉线长短不同.
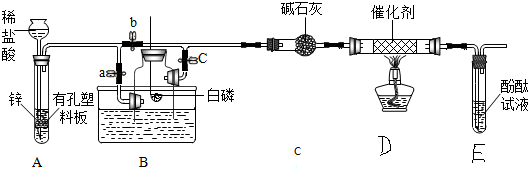
【发现问题2】同学们用蜡烛代替红磷测定空气中氧气的含量,发现蜡烛很快熄灭,回流到集气瓶中的水远小于瓶容积的$\frac{1}{5}$.是什么原因所致呢?
【猜想与假设2】猜想①:蜡烛燃烧产生CO2气体;
猜想②:装置漏气;
猜想③:没有冷却至室温.
【实验验证】将蜡烛点燃后用氧气传感器定量测定瓶中的氧气含量.数据如图.
【得出结论】此实验中空气中氧气体积分数降低了5.18%.
【深入探究】蜡烛燃烧产生的CO2可能是影响蜡烛熄灭的主要原因.
请你设计方案除去集气瓶中蜡烛燃烧生成的CO2方案中化学方程式2NaOH+CO2=Na2CO3+H2O.
【拓展探究】某同学用氧气传感器定量测定密闭条件下足量红磷燃烧时氧气的含量变化,如图,在110秒时
氧气的含量有所上升,接着再慢慢下降,最终维持在8.85%左右.请你试着解释图象变化的可能原因是:
①红磷燃烧放出热量使得氧气体积膨胀;
②装置漏气,空气进入装置.
你对氧气含量最终维持在 8.85%左右是怎么理解的?
分析 【猜想与假设1】根据影响燃烧的剧烈程度的因素来分析;
【猜想与假设2】根据发现的问题以及实验装置来分析可能的原因;
【得出结论】根据反应前后氧气含量的数据来分析;
【深入探究】
(1)根据二氧化碳的性质以及反应过程来分析解答;
(2)红磷燃烧放出热量,导致氧气体积膨胀或装置漏气;
氧气含量过低,红磷不能发生燃烧.
磷与氧气在点燃的条件下反应生成五氧化二磷.
解答 解:【猜想与假设1】可能与蜡烛烛心棉线的长短有关,棉线越长,与空气的接触面越大,燃烧也越旺盛,故填:蜡烛烛心棉线长短不同;
【猜想与假设2】蜡烛熄灭后,进入的水的体积远小于瓶子容积的五分之一,可能是蜡烛燃烧生成了二氧化碳,还可能是装置漏气或没有冷却至室温,蜡烛燃烧需要一定的氧气,故填:装置漏气;没有冷却至室温;
【得出结论】反应前,装置内空气中氧气的体积分数约为21%,蜡烛熄灭后,瓶内氧气的含量为15.82%,此实验中空气中氧气体积分数降低了:21%-15.82%=5.18%;故填:5.18;
【深入探究】
(1)二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,故填:在实验前,瓶内加入少量的浓氢氧化钠溶液;2NaOH+CO2=Na2CO3+H2O;
(2)在110秒时氧气的含量有所上升,接着再慢慢下降,可能是红磷燃烧放出热量使得氧气体积膨胀或装置漏气,空气进入装置;故填:红磷燃烧放出热量使得氧气体积膨胀;装置漏气,空气进入装置;
当装置的氧气含量低到8.85%时,红磷就不能继续燃烧而熄灭,所以氧气的含量最终维持在8.85%左右;故填:当装置的氧气含量低到8.85%时,红磷就不能继续燃烧而熄灭;
答案:
【猜想与假设1】蜡烛烛心棉线长短不同;
【猜想与假设2】②装置漏气;③没有冷却至室温;
【得出结论】5.18;
【深入探究】在实验前,瓶内加入少量的浓氢氧化钠溶液,燃烧后振荡集气瓶;2NaOH+CO2=Na2CO3+H2O;
【拓展研究】红磷燃烧放出热量使得氧气体积膨胀;装置漏气,空气进入装置;
当装置的氧气含量低到8.85%时,红磷就不能继续燃烧而熄灭,所以氧气的含量最终维持在8.85%左右.
点评 本题主要考查用蜡烛、红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案 X、Y两种固体(均不带结晶水)物质的溶解度曲线如图所示,下列有关叙述正确的是( )
X、Y两种固体(均不带结晶水)物质的溶解度曲线如图所示,下列有关叙述正确的是( )| A. | t2℃时,用160g X的饱和溶液加水可以配成500g12.5%的X溶液 | |
| B. | t2℃时,X和Y的两杯饱和溶液降到t1℃,析出的X一定比Y多 | |
| C. | 向M点65g X溶液中加入15g X固体能得到t2℃X的饱和溶液 | |
| D. | t1℃时,X和Y的饱和溶液升到t2℃,溶质的质量分数都增大 |
| A. | 棉花和羊毛的主要成分都是蛋白质 | |
| B. | 塑料是最常见的有机合成材料,具有密度小、耐腐蚀、易加工等优点 | |
| C. | 聚乙烯、聚氯乙烯都可用于包装食品 | |
| D. | 钛合金、玻璃钢、碳纤维复合材料等都属于复合材料 |
 某研究小组发现,维C泡腾片(保健品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究:
某研究小组发现,维C泡腾片(保健品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究:探究一:该气体的成分.
【猜想与假设】
小华说:该气体可能是CO2、O2、CO、H2、N2中的一种或几种.
小明说:不可能含有N2,因为:根据质量守恒定律(或化学反应前后元素种类不变),反应物中不含氮元素
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒
经讨论,最后该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(1)由实验①可知,该气体中肯定含有二氧化碳,写出该反应的化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.
探究二:维C泡腾片溶液的酸碱性.
向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性.
【拓展延伸】人体缺乏维生素C会引起坏血病.
| A. | 实验记录:①用10mL量筒量取7.02mL水; ②用托盘天平称取5.6g氯化钠 | |
| B. | 安全常识:①酒精灯打翻起火,用湿抹布扑灭; ②冬天用煤炉取暖,应保证室内通风 | |
| C. | 化学与健康:①人体缺维生素A会引起夜盲症; ②禁止使用任何食品添加剂 | |
| D. | 化学与生活:①用钢丝球擦洗铝锅上的污垢; ②用食醋除水垢 |
| A. | K2MnO4 | B. | KMnO4 | C. | Mn(OH)2 | D. | Mn2O7 |
| A. | 服用含氢氧化铝的药物治疗胃酸过多 Al(OH)3+3HCl═AlCl3+H2O 复分解反应 | |
| B. | 拉瓦锡研究空气成分 2Hg0$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+02↑ 分解反应 | |
| C. | 用天然气作燃料 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 验证铜和铝的活动性 Cu+AlS04═CuS04+Al 置换反应 |