题目内容
10.某化学兴趣小组对“怎样验证没有明显现象的化学反应是否发生”进行了如下探究.
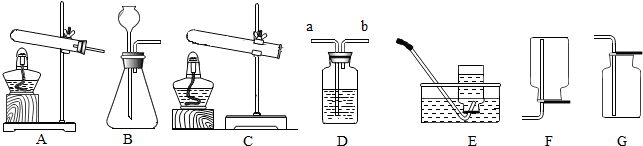
[探究实验一]如图1所示,向左、右两管中同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸,开始时左管溶液呈红色.一段时间后U型管中溶液全部呈无色,证明了氢氧化钠与稀盐酸发生了反应.请写出上述反应的化学方程式NaOH+HCl═NaCl+H2O.
[探究实验二]如图2所示,在两个体积相同的A、B软塑料瓶内先先充满CO2,然后分别倒入等体积的饱和NaOH溶液和水,迅速拧紧瓶盖振荡,可观察到A软塑料瓶明显变扁,证明了氢氧化钠与二氧化碳发生了反应.
(1)A中发生反应的化学方程式为CO2+2NaOH═Na2CO3+H2O.
(2)B瓶的作用是对比.
[探究实验三]
| 实验步骤 | 实验现象 | 结论 |
| 取图2实验中A瓶反应后所得的溶液少许于试管中,再向试管中滴加稀盐酸溶液 | 有气泡产生 | 验证了二氧化碳和氢氧化钠溶液发生了反应 |
①可以借助酸碱指示剂证明反应的发生;
②通过检验生成物证明反应的发生.
分析 [探究实验一]根据酸碱指示剂的性质进行分析,酚酞遇碱变红,遇酸性和中性溶液不变色.氢氧化钠和盐酸反应生成氯化钠和水.
[探究实验二]根据二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,使瓶内压强变小,据此进行分析解答;
[探究实验三]要证明塑料瓶中发生了化学反应,可证明有碳酸钠生成,碳酸钠能与稀盐酸反应生成二氧化碳气体,据此进行分析解答;
【反思拓展】根据通过以上实验可以看出,对于没有明显现象的化学反应,我们可以通过检验反应物是否减少或检验生成物的方法验证反应是否发生解答;
解答 解:
[探究实验一]氢氧化钠呈碱性,能使酚酞变红,稀盐酸呈酸性,使酚酞试液不变色,故开始时右边溶液为无色,左边溶液为红色;
氢氧化钠与盐酸反应方程式为:NaOH+HCl═NaCl+H2O;
[探究实验二]向甲、乙两瓶中分别倒入相同体积的蒸馏水和氢氧化钠溶液,然后将两瓶迅速拧紧瓶盖,振荡,观察现象.该实验的探究目的是氢氧化钠溶液能吸收更多的二氧化碳;二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,使瓶内压强变小,会观察到塑料瓶变瘪了;反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
[探究实验三]证明塑料瓶中发生了化学反应,可证明有碳酸钠生成,碳酸钠能与稀盐酸反应生成二氧化碳气体,故可向瓶中加入稀盐酸,有气泡产生,证明塑料瓶中发生了化学反应.
【反思拓展】通过以上实验可以看出,对于没有明显现象的化学反应,我们可以通过检验反应物是否减少或检验生成物的方法验证反应是否发生;
答案:
[探究实验一]左 NaOH+HCl═NaCl+H2O
[探究实验二](1)CO2+2NaOH═Na2CO3+H2O 对比
[探究实验三]
| 实验步骤 | 实验现象 | 结论 |
| 取图2实验中A瓶反应后所得的溶液少许于试管中,再向试管中滴加 稀盐酸溶液 | 有气泡产生 | 验证了二氧化碳和氢氧化钠溶液发生了反应 |
点评 本题考查了酸碱指示剂的变色情况,完成此题,可以依据已有的知识进行.本题难度不大,掌握碱的化学性质、碳酸盐的检验方法等是正确解答本题的关键.对比实验、反应物检验是探究无明显现象反应是否发生的常用方法.

 名校课堂系列答案
名校课堂系列答案| A. | 几千成年前地球上一条恐龙体内某个原子可能在你的身体里 | |
| B. | 当个人实验结果与多数人不同时,应查找原因,重复实验 | |
| C. | 用刀切西瓜的过程中,个别原子被分成了更小的微粒 | |
| D. | 化学是在原子、分子水平上研究物质的组成、性质的变化规律 |
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(2)20℃时,NaOH的溶解度为91g.
(3)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体的措施有:①加入氢氧化钙,②升高温度,③减低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰.其中正确的是D.
A.②④⑥B.③④C.①③⑤⑥D.①②⑤⑥
(4)现将20℃时Ca(OH)2的饱和溶液甲溶液降温至0℃得到乙溶液,则两种溶液中溶质的质量分数相比,乙=(填“>”“<”或“=”)甲.
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶并过滤.

 水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.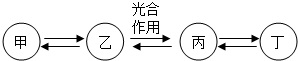 如图中的甲、乙、丙、丁四种物质均含氧元素,甲中碳的质量分数为12%,丙是单质.甲转化为乙的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;丁分解为丙的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;丙的一种用途是供给呼吸.
如图中的甲、乙、丙、丁四种物质均含氧元素,甲中碳的质量分数为12%,丙是单质.甲转化为乙的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;丁分解为丙的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;丙的一种用途是供给呼吸.