题目内容
18.某校化学兴趣小组学习了气体的制取和收集后,对相关知识进行总结,请你一起参与,并完成下面题目内容:
(1)写出仪器a名称:
(2)实验室若用氯酸钾和二氧化锰制取纯净的氧气,应选用的装置组合AD(填字母符号,下同),反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.二氧化锰在反应前后固体混合物中的质量分数将变大(填“变大”、“变小”或“不变”).
(3)实验室制取CO2的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.若用G装置收集二氧化碳,则应从b(填“a”或“b”)端进气.
(4)实验室用锌粒和稀硫酸反应制取氢气,发生装置选择C优点是能使反应随时进行或停止打开止水夹,若发现稀硫酸未能与多孔隔板上的锌粒接触,但此时已无稀硫酸可加,在不影响氢气总量的前提下,下列溶液中,可以从长颈漏斗中添加的是.
A.氢氧化钠溶液 B.碳酸钠溶液 C.硫酸钠溶液 D.氯化钡溶液.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
氧气的密度比空气的密度大,不易溶于水;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大;
(4)不同的实验装置,功能不同;
氢氧化钠和碳酸钠能和稀硫酸反应,氯化钡和稀硫酸反应生成硫酸钡沉淀和稀盐酸.
解答 解:(1)仪器a是长颈漏斗,通过长颈漏斗可以向反应容器中注入液体药品;
(2)实验室用氯酸钾和二氧化锰制取氧气时需要加热,应该用A装置作为发生装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用E装置收集,氧气不易溶于水,可以用排水法收集,即用D装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净;
反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
二氧化锰在反应前后的质量不变,而固体的总质量减小,因此二氧化锰在固体混合物中的质量分数将变大;
(3)实验室制取CO2的化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;
若用G装置收集二氧化碳,由于二氧化碳的密度比空气大,则应从b端进气;
(4)实验室用锌粒和稀硫酸反应制取氢气,发生装置选择C优点是能使反应随时进行或停止,原理是:关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止;
打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行.
氢氧化钠和碳酸钠能够消耗稀硫酸,因此能够影响氢气总量;
硫酸钠不能和稀硫酸反应,氯化钡虽然能和稀硫酸反应,但是能够生成稀盐酸,因此不影响氢气总量,因此在不影响氢气总量的前提下,下列溶液中,可以从长颈漏斗中添加的是硫酸钠溶液和氯化钡溶液.
故答案为:长颈漏斗;AD;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;变大;CaCO3+2HCl═CaCl2+H2O+CO2↑;b;能使反应随时进行或停止;CD.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 名校课堂系列答案
名校课堂系列答案| A. | 肥皂水可以区别硬水和软水 | |
| B. | 计算机房失火只能用泡沫灭火器灭火 | |
| C. | 风力发电可以减少对环境的污染 | |
| D. | 不能将固体废弃物扔到深山老林中 |
| A. | 加入盐酸,有无色气体产生的物质中一定含有碳酸盐 | |
| B. | 有机物中一定含碳元素,因此含有碳元素的化合物一定是有机物 | |
| C. | 向某无色溶液中滴加酚酞,酚酞变红,该溶液一定是碱溶液 | |
| D. | 某物质在氧气中燃烧能生成水,该物质中一定含有氢元素 |
| A. |  紫砂壶 | B. |  塑料篮 | C. |  真丝围巾 | D. |  铝合金物品 |

[探究实验一]如图1所示,向左、右两管中同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸,开始时左管溶液呈红色.一段时间后U型管中溶液全部呈无色,证明了氢氧化钠与稀盐酸发生了反应.请写出上述反应的化学方程式NaOH+HCl═NaCl+H2O.
[探究实验二]如图2所示,在两个体积相同的A、B软塑料瓶内先先充满CO2,然后分别倒入等体积的饱和NaOH溶液和水,迅速拧紧瓶盖振荡,可观察到A软塑料瓶明显变扁,证明了氢氧化钠与二氧化碳发生了反应.
(1)A中发生反应的化学方程式为CO2+2NaOH═Na2CO3+H2O.
(2)B瓶的作用是对比.
[探究实验三]
| 实验步骤 | 实验现象 | 结论 |
| 取图2实验中A瓶反应后所得的溶液少许于试管中,再向试管中滴加稀盐酸溶液 | 有气泡产生 | 验证了二氧化碳和氢氧化钠溶液发生了反应 |
①可以借助酸碱指示剂证明反应的发生;
②通过检验生成物证明反应的发生.
(1)各取2mL溶液于试管中,分别滴入Na2CO3溶液,现象溶液变浑浊,是Ca(OH)2溶液,反应的化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(2)各取2mL溶液于试管中,通入CO2也能鉴别出来.若不采用化学药品制取CO2,则我的操作是用玻璃管分别向溶液中吹气.
(3)NaOH溶液中通入CO2无明显变化,在反应后的溶液中加入下列物质仍不能证明NaOH与CO2反应的是C.
A、稀盐酸 B、Ba(OH)2溶液 C、酚酞溶液
(4)NaOH溶液中通入少量的CO2后,所得溶液的溶质:可能是Na2CO3,也可能是Na2CO3和NaOH的混合物.
| 操 作 | 现 象 | 结论 |
| ①向反应后的溶液中加入足量的氯化钙溶液; | 溶液变浑浊 | 溶质是 Na2CO3 |
| ②静置后,用玻璃棒蘸取上层清液,滴在pH试纸上. | pH=7 |
 目前,电动车以其小巧轻便而成为普通市民的代步工具(如图所示).
目前,电动车以其小巧轻便而成为普通市民的代步工具(如图所示).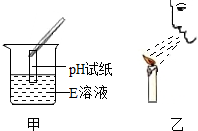 甲、乙两位同学做如下两个实验,请回答:
甲、乙两位同学做如下两个实验,请回答: