题目内容
12.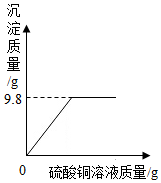 向一定量的氢氧化钠溶液中逐渐加入硫酸铜溶液,生成硫酸钠和氢氧化铜沉淀,测得生成沉淀的质量与所加硫酸铜溶液的质量关系如图所示.
向一定量的氢氧化钠溶液中逐渐加入硫酸铜溶液,生成硫酸钠和氢氧化铜沉淀,测得生成沉淀的质量与所加硫酸铜溶液的质量关系如图所示.(1)反应后生成沉淀的质量为9.8g.
(2)当两种溶液恰好完全反应时,测得所得溶液质量为142g,试计算所得溶液中溶质的质量分数.
分析 硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,根据生成沉淀的质量与所加硫酸铜溶液的质量关系图分析生成的氢氧化铜的沉淀,由反应生成沉淀的质量可以计算硫酸钠的质量,进一步可以计算所得溶液中溶质硫酸钠的质量分数.
解答 解:(1)由生成沉淀的质量与所加硫酸铜溶液的质量关系图可知,反应后生成沉淀的质量为9.8g;
(2)设反应生成的硫酸钠的质量为x
2NaOH+CuSO4═Na2SO4+Cu(OH)2↓
142 98
x 9.8g
$\frac{142}{98}=\frac{x}{9.8g}$ 解得:x=14.2g
所得溶液中溶质的质量分数是:$\frac{14.2g}{142g}×100%$=10%
故答为:(1)9.8;(2)所得溶液中溶质的质量分数是10%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
3.钾长石是一种金属矿物,其主要成分的化学式为KAlSi3O8,其中硅元素的化合价为( )
| A. | -4 | B. | +2 | C. | +4 | D. | +6 |
20.某同学测得一些食物的近似pH如下,其中酸性最强的是( )
| A. | 苹果汁:3.1 | B. | 玉米粥:7.5 | C. | 牛奶:6.5 | D. | 番茄汁:4.2 |
17.分类法是化学学习的重要方法之一.下列各组物质按照单质、盐、混合物顺序排列的是( )
| A. | 铁、氢氧化铜、冰水混合物 | B. | 液氧、硫酸钡、食盐水 | ||
| C. | 天然气、纯碱、石油 | D. | 水银、氯化镁、海水 |
4.下列物质中,氮和氧的质量之比为7:20的是( )
| A. | N2O | B. | NO | C. | NO2 | D. | N2O5 |
1.在反应X+2Y=R+2M中,当1.6gX与Y完全反应后,生成4.4gR,且反应生成的R和M的质量之比为11:9,则在此反应中Y和M的质量之比( )
| A. | 1:9 | B. | 2:9 | C. | 16:9 | D. | 23:9 |
