题目内容
8.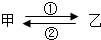 甲、乙是初中化学常见的物质,它们在一定条件下能如图所示相互转化.
甲、乙是初中化学常见的物质,它们在一定条件下能如图所示相互转化.(1)若甲能供给呼吸,乙为无色液体,反应②的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,基本反应类型是分解反应;
(2)若甲、乙均是某非金属元素的气态氧化物,甲有毒,反应①的化学方程式为2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2(合理即可).
分析 (1)甲能供给呼吸,则甲为氧气,水为无色液体,氧气能与水在一定条件下相互转化,据此进行分析解答.
(2)甲、乙均是某非金属元素的气态氧化物,甲有毒,则甲为一氧化碳,一氧化碳与二氧化碳在一定条件下相互转化,据此进行分析解答.
解答 解:(1)甲能供给呼吸,则甲为氧气,水为无色液体,氧气能与水在一定条件下相互转化,反应②是水生成氧气,水通电分解能生成氢气和氧气,该反应符合“一变多”的特征,属于分解反应;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;分解反应;
(2)甲、乙均是某非金属元素的气态氧化物,甲有毒,则甲为一氧化碳,一氧化碳与二氧化碳在一定条件下相互转化,则乙为二氧化碳;反应①是一氧化碳在点燃条件下生成二氧化碳,故反应的化学方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2(合理即可).
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
相关题目
5.下列各组物质的化学式、名称和分类三者不正确的是( )
| A. | CaO、生石灰、氧化物 | B. | CH4、沼气、有机物 | ||
| C. | Na2CO3、纯碱、碱 | D. | H3PO4、磷酸、酸 |
16.CO2、CH4 和氮氧化合物都是形成温室效应的气体.下列减缓全球气候变暖的对策中,不恰当的是( )
| A. | 在某些工业生产过程中,将欲排放的CO2用化学试剂吸收 | |
| B. | 禁止制备和使用CH4和氮氧化合物等温室气体 | |
| C. | 开发无污染的太阳能、风能、地热能等 | |
| D. | 变革能源消耗模式 |
13.某校化学兴趣小组对某化学反应进行了探究,实验测定结果如下,
下列有关说法正确的是( )
| 物 质 | A | B | C | D |
| 反应前质量/g | 20 | 12 | 2 | 6 |
| 反应后质量/g | 0 | 2 | 2 | 待测 |
| A. | 该反应是分解反应 | B. | 反应后D物质的质量是30 g | ||
| C. | C物质可能是该反应的催化剂 | D. | B物质全部参加反应 |
20.下列知识归纳,完全正确的一组是( )
| A.燃烧条件 | B.认识粒子 |
| ①可燃物 ②氧气(或空气) ③温度达到着火点 | ①原子比分子小 ②分子运动原子不运动 ③分子由原子构成 |
| C.化学元素 | D.化学之最 |
| ①缺铁可能导致贫血 ②缺钙可能导致弱智 ③缺碘可能导致佝偻病 | ①熔点最低的金属是汞 ②地壳中含量最多的元素是氧 ③导电性最好的金属是铜 |
| A. | 燃烧条件 | B. | 认识粒子 | C. | 化学元素 | D. | 化学之最 |
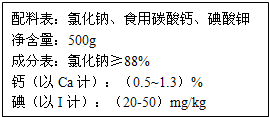 如图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算.
如图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算.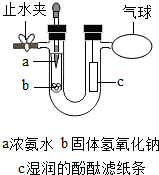 某同学在学完《分子和原子》后,对教材中的实验进行了如图改进:
某同学在学完《分子和原子》后,对教材中的实验进行了如图改进: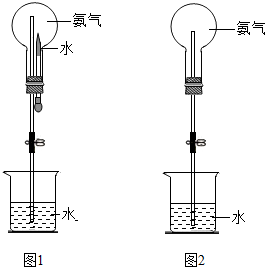 我国化学家侯德榜于1923年研制成功的“联合制碱法(又称侯氏制碱法)”的主要特点是:在浓氨水(NH3极易溶于水)中通入足量的二氧化碳生成一种盐,然后在此溶液中加入细的食盐粉末,由于NaHCO3在该状态下溶解度很小,呈晶体析出,同时由于大部分酸式碳酸盐加热容易转变为正盐,所以将析出的NaHCO3加热分解即可得纯碱,请回答:
我国化学家侯德榜于1923年研制成功的“联合制碱法(又称侯氏制碱法)”的主要特点是:在浓氨水(NH3极易溶于水)中通入足量的二氧化碳生成一种盐,然后在此溶液中加入细的食盐粉末,由于NaHCO3在该状态下溶解度很小,呈晶体析出,同时由于大部分酸式碳酸盐加热容易转变为正盐,所以将析出的NaHCO3加热分解即可得纯碱,请回答: