题目内容
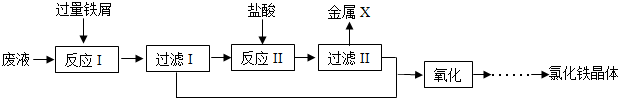
 “侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠.某化学兴趣小组的同学拟测定某纯碱样品中Na2CO3的质量分数.
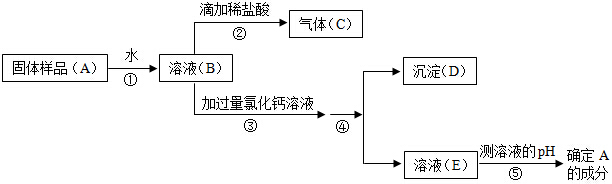
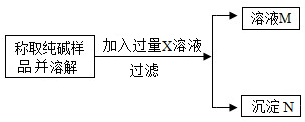
“侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠.某化学兴趣小组的同学拟测定某纯碱样品中Na2CO3的质量分数.【方案一】沉淀分析法(如图所示).
(1)溶液M含有的溶质是CaCl2和
【方案二】气体分析法
称取该纯碱样品21.5g,加入到盛有150g的稀盐酸的烧杯中,样品完全反应后,测得烧杯内混合物的质量为162.7g.
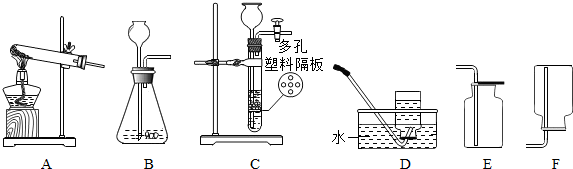
(2)写出实验室检验反应中生成气体的化学方程式:
(3)求该纯碱样品中Na2CO3的质量分数.(写出具体计算过程)
(4)假如称量准确,通过计算得到的纯碱样品中Na2CO3的质量分数比实际数值偏小,你认为其中可能的原因是
考点:实验探究物质的组成成分以及含量,盐的化学性质,根据化学反应方程式的计算
专题:科学探究
分析:【方案一】(1)根据溶液M含有的溶质是CaCl2说明加入x的溶液是氯化钙溶液,氯化钙和碳酸钠反应生成氯化钠和碳酸钙沉淀,故溶液M含有的溶质是CaCl2和NaCl,沉淀N的化学式是CaCO3
【方案二】
(2)碳酸钠和稀盐酸反应生成氯化钠、水、二氧化碳,二氧化碳通常用澄清的石灰水检验,写出反应的化学方程式;
(3)根据题中信息解答;
(4)根据部分CO2 溶于水解答.
【方案二】
(2)碳酸钠和稀盐酸反应生成氯化钠、水、二氧化碳,二氧化碳通常用澄清的石灰水检验,写出反应的化学方程式;
(3)根据题中信息解答;
(4)根据部分CO2 溶于水解答.
解答:解:
【方案一】
(1)溶液M含有的溶质是CaCl2说明加入x的溶液是氯化钙溶液,样品中的氯化钠和氯化钙不反应,由于氯化钙过量,因此碳酸钠完全反应,且生成了氯化钠,因此溶液M中含有的溶质是CaCl2和NaCl,沉淀N的化学式是CaCO3
【方案二】
(2)碳酸钠和稀盐酸反应生成氯化钠、水、二氧化碳,二氧化碳通常用澄清的石灰水检验,反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O
(3)设Na2CO3的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 8.8g
106:44=x:8.8g
x=21.2g
×100%=98.6%
(4)由于部分CO2 溶于水,因此通过计算得到的纯碱样品中Na2CO3的质量分数比实际数值偏小.
答案:
(1)NaCl CaCO3
(2)Ca(OH)2+CO2=CaCO3↓+H2O
(3)该纯碱样品中Na2CO3的质量分数为98.6%
(4)部分CO2 溶于水
【方案一】
(1)溶液M含有的溶质是CaCl2说明加入x的溶液是氯化钙溶液,样品中的氯化钠和氯化钙不反应,由于氯化钙过量,因此碳酸钠完全反应,且生成了氯化钠,因此溶液M中含有的溶质是CaCl2和NaCl,沉淀N的化学式是CaCO3
【方案二】
(2)碳酸钠和稀盐酸反应生成氯化钠、水、二氧化碳,二氧化碳通常用澄清的石灰水检验,反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O
(3)设Na2CO3的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 8.8g
106:44=x:8.8g
x=21.2g
| 21.2g |
| 21.5g |
(4)由于部分CO2 溶于水,因此通过计算得到的纯碱样品中Na2CO3的质量分数比实际数值偏小.
答案:
(1)NaCl CaCO3
(2)Ca(OH)2+CO2=CaCO3↓+H2O
(3)该纯碱样品中Na2CO3的质量分数为98.6%
(4)部分CO2 溶于水
点评:本题难度太大,考查了多方面的化学知识,要想做对此题必须知识全面,再加上足够的细心和耐心才行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目