题目内容
7.2011年3月,日本地震引发福岛第一核电站的放射性物质碘-131外泄.人体的甲状腺会吸收放射性碘-131,并对甲状腺造成损伤.碘片可减少甲状腺对碘-131的吸收.请回答下列问题
(1)碘片中的“碘”指的是元素(选填“分子”,“原子”或“元素”).
(2)碘-131原子的原子核带53个单位的正电荷,则该原子的核外电子数为53.
分析 (1)根据碘的存在来分析碘片中的“碘”;
(2)根据原子中质子数等于核外电子数来解答.
解答 解:(1)因碘片中的“碘”是存在于化合物中,则是指碘元素,故答案为:元素;
(2)由碘-131原子的原子核带53个单位的正电荷,因质子带正电,则质子数为53,又原子中质子数等于核外电子数,即该原子的核外电子数为53,故答案为:53.
点评 本题属于信息习题,学生应注意信息的抽取,并学会利用信息和所学知识来解决问题,注重了知识的迁移和基础知识的应用.

练习册系列答案
相关题目
17.“千里之行,始于足下”.汽车是常用的交通工具,但汽车尾气会造成空气污染.下列能源的使用最有利于防止空气污染的是( )
| A. | 天然气 | B. | 太阳能 | C. | 汽油 | D. | 柴油 |
18.下表中,有关量的变化图象与其对应叙述相符的是( )
| A. | 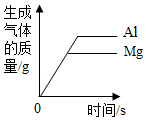 等质量的铝和镁分别与足量的等溶质质量分数的稀硫酸充分反应 等质量的铝和镁分别与足量的等溶质质量分数的稀硫酸充分反应 | |
| B. | 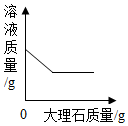 向一定质量的稀盐酸中加入大理石 向一定质量的稀盐酸中加入大理石 | |
| C. | 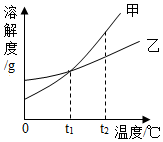 将甲、乙两种物质的饱和溶液分别从t2℃降温至t1℃时,析出晶体的质量甲不一定大于乙 将甲、乙两种物质的饱和溶液分别从t2℃降温至t1℃时,析出晶体的质量甲不一定大于乙 | |
| D. | 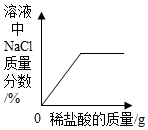 向一定质量的氢氧化钠溶液中加入稀盐酸 向一定质量的氢氧化钠溶液中加入稀盐酸 |
2.向盛有10mL稀盐酸(其中滴有少量紫色石蕊试剂)的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下.请分析并回答下列问题:
(1)当加入氢氧化钠溶液的体积为10mL时,稀盐酸和氢氧化钠溶液恰好完全反应;
(2)请你写出此过程中发生的化学反应方程式NaOH+HCl=NaCl+H2O.
(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有哪些?NaCl和HCl(或氯化钠和氯化氢).
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
(2)请你写出此过程中发生的化学反应方程式NaOH+HCl=NaCl+H2O.
(3)当烧杯中溶液的pH=1.4时,溶液中的溶质有哪些?NaCl和HCl(或氯化钠和氯化氢).
12.某科学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
(1)从以上数据可知,最后剩余的0.6g固体的成分是铜;
(2)计算合金样品中镁的质量分数.
(3)计算所用稀硫酸中H2SO4的质量分数.
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | 2.5g |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
(2)计算合金样品中镁的质量分数.
(3)计算所用稀硫酸中H2SO4的质量分数.
19.在元旦晚会上小明表演了-个魔术:他拿出一把装满“水”的“宝壶”,分别向编号为ABCDEF六只烧杯(装有少量不同试剂)中倒“水”,结果A杯无色透明,B杯看似红墨水,C杯看似蓝墨水,D杯看似牛奶,E杯看似红褐色涂料,F杯看似蓝色果冻.则宝壶中的“水”可能是( )
| A. | NaOH溶液 | B. | HCl溶液 | C. | CuSO4溶液 | D. | FeCl3溶液 |
