题目内容
7.合金的用途十分广泛.某化学小组欲测定黄铜片(铜锌合金)的组成进行如下实验:取黄铜片30g放入烧杯,将250g稀硫酸分5次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算:| 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 23.5 | 17 | 10.5 | 9.6 | 9.6 |
(2)稀硫酸中溶质的质量分数.
分析 根据锌会与硫酸反应生成硫酸锌和氢气,铜不会与稀硫酸反应,依据题中的数据进行计算.
解答 解:由表中数据知,合金中铜的质量为9.6g,其含量为:$\frac{9.6g}{30g}$×100%=32%,
与50g稀硫酸完全反应消耗锌的质量为:30g-23.5g=6.5g,
设与6.5g锌反应的硫酸的质量为x,
Zn+H2SO4=ZnSO4+H2↑,
65 98
6.5g x
$\frac{65}{6.5g}$=$\frac{98}{x}$
x=9.8g
硫酸中溶质的质量分数为:$\frac{9.8g}{50g}$×100%═19.6%
故答案为:黄铜片中铜的含量是32%,稀硫酸中溶质的质量分数是19.6%.
点评 本题主要考查化学方程式进行计算,计算时要注意规范性和准确性.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
16.下列操作中发生复分解反应的是( )
| A. | 将碳酸钾加入氯化钠溶液中 | B. | 在硫酸铜溶液中加入铁片 | ||
| C. | 在盐酸中加入氢氧化钠溶液 | D. | 让铁丝在氧气中燃烧 |
15.某化学实验小组的同学对实验室2瓶氢氧化钠固体产生了兴趣,为探究其成分进行了有关实验.请你参与他们进行的探究活动:
【提出问题】久置氢氧化钠固体的成分是什么?
【猜想与假设】猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:NaOH和Na2CO3
【实验与探究】
(1)实验如下:
(2)为了进一步的验证猜想结果,小明同学提出如下实验方案:继续实验二,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则此瓶中猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立.
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈碱性(填“酸”或“碱”),能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是滴加过量的氯化钡溶液
【反思与交流】久置的固体氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH═Na2CO3+H2O.
【提出问题】久置氢氧化钠固体的成分是什么?
【猜想与假设】猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:NaOH和Na2CO3
【实验与探究】
(1)实验如下:
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 实验一:取其中一瓶的少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的稀盐酸. | 实验过程中始终没有气泡产生. | 则证明此瓶中猜想Ⅰ成立. |
| 实验二:取另一瓶中的少量固体样品于试管中,加蒸馏水完全溶解,然后滴加少量氯化钡溶液. | 实验过程中产生 白色沉淀 | 则证明猜想Ⅱ或Ⅲ成立. 此过程中发生反应的化学方程式为BaCl2+Na2CO3═BaCO3↓+2NaCl |
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈碱性(填“酸”或“碱”),能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是滴加过量的氯化钡溶液
【反思与交流】久置的固体氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH═Na2CO3+H2O.
2.2016年3月22日是第二十四届“世界水日”,3月22-28日是第二十九届“中国水周”.联合国确定2016年“世界水日”的宣传主题是“水与就业”(Water and Jobs).经研究确定,我国纪念2016年“世界水日”和“中国水周”活动的宣传主题为“落实五大发展理念,推进最严格水资源管理”.下列跟水有关的变化中没有化学变化的是( )
| A. | 水的净化 | B. | 太阳能分解水制氢气 | ||
| C. | 海水晒盐 | D. | 肥皂水区分硬水和软水 |
19.一些大型化工企业选择在远离城市的长江下游沿岸建厂,下述理由错误的是( )
| A. | 化工企业需要大量的水 | |
| B. | 便于向长江内大量排污水 | |
| C. | 便于原材料和产品的运输 | |
| D. | 减少化工企业生产过程中三废对人口稠密地区的危害 |
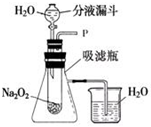 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.