题目内容
6.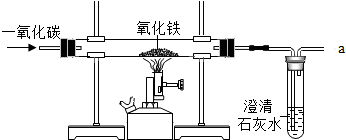 炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见如图.
炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见如图.请你对实验进行分析并回答:
(1)给玻璃管加热的仪器叫酒精喷灯,要用其外焰(填“外焰”、“内焰”或“焰心”)进行加热.
(2)实验中玻璃管里氧化铁粉末的颜色变化是由红棕色逐渐变为黑色,反应的化学方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)实验前先通入CO,后再开始加热,实验后先停止加热,后再停止通入CO的原因而是(答一点)除去装置中的空气,以免加热时装置发生爆炸(或作保护气,以免生成的铁在高温下被氧化).
(4)实验要在装置末端a处燃着一盏酒精灯,其作用是除去尾气中的一氧化碳,以免一氧化碳污染空气.
分析 (1)根据酒精喷灯火焰各部分的温度分析;
(2)根据反应物和生成物,分析实验中玻璃管里氧化铁粉末的颜色变化.并书写方程式;
(3)根据玻璃管内有空气,通入一氧化碳易发生爆炸分析;根据还原出的铁温度较高,易于空气中的氧气反应重新生成铁的氧化物分析;
(4)根据一氧化碳是对大气有污染的气体分析.
解答 解:(1)由于酒精喷灯的外焰的温度最高,加热时要用外焰进行加热;故填:外焰;
(2)由于在高温下,一氧化碳将氧化铁还原为铁,同时生成了二氧化碳.所以可以观察到实验中玻璃管里氧化铁粉末的颜色变化是红色粉末变黑色;故填:固体粉末由红棕色逐渐变为黑色;3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)由于玻璃管内有空气,通入一氧化碳高温时易发生爆炸.所以,实验前先通入CO,排净玻璃管中的空气再开始加热;由于还原出的铁温度较高,易于空气中的氧气反应重新生成铁的氧化物.所以,实验后先停止加热再停止通入CO,直到玻璃管冷却为止;
故填:除去装置中的空气,以免加热时装置发生爆炸(或作保护气,以免生成的铁在高温下被氧化);
(4)为了防止一氧化碳对大气的污染,所以,实验时要在装置末端a处燃着一盏酒精灯除去反应剩余的CO;
故填:除去尾气中的一氧化碳,以免一氧化碳污染空气.
点评 本题主要考查一氧化碳与氧化铁反应实验装置、实验现象、一氧化碳的化学性质和反应原理以及环保的问题,细心分析即可.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
14.物质是由微粒构成的,用化学知识分析比较下来微粒结构的异同点:
| H2O、H2O2和NH3 | 相同之处:(写两条)①都属于化合物;②都含有氢元素 |
Na+ 与F 与F | 不同之处:(写两条)①最外层电子数不同;②质子数 |
11.在10.4克H2O2溶液中加入1g二氧化锰,充分反应后,生成氧气的质量为3.2克,则原溶液中含有氧元素( )
| A. | 9.6克 | B. | 8.8克 | C. | 4.2克 | D. | 3.2克 |
18.一些食物的近似pH值如下表:
请回答下列问题:
(1)苹果汁和葡萄汁相比较,酸性较强的是A(填字母编号)
(2))治疗胃酸过多的药物之一是胃舒平药片,其主要成分是氢氧化铝[Al(OH)3],请用化学方程式表示它与胃酸作用的原理Al(OH)3+3HCl=AlCl3+3H2O.
| 食物 | A.苹果 | B.葡萄 | C.牛奶 | D.玉米粥 |
| pH | 2.9-3.3 | 3.5-4.5 | 6.3-6.6 | 6.8-8.0 |
(1)苹果汁和葡萄汁相比较,酸性较强的是A(填字母编号)
(2))治疗胃酸过多的药物之一是胃舒平药片,其主要成分是氢氧化铝[Al(OH)3],请用化学方程式表示它与胃酸作用的原理Al(OH)3+3HCl=AlCl3+3H2O.
16.燃煤产生的烟气中含有二氧化硫,直接排放会污染空气,它与水反应形成酸雨污染环境,某科研小组利用海水除去二氧化硫,其工艺流程如图:

请回答下列问题:
(1)用熟石灰中和稀硫酸的化学方程式是Ca(OH)2+H2SO4═CaSO4+2H2O.
(2)为了研究脱硫率(脱硫率是已除去的二氧化硫的量占二氧化硫总量的百分比)与温度、烟气中SO2浓度的关系,他们进行了探究实验.实验结果如下:
由表中实验数据可得出的结论是浓度一定时,温度升高,脱硫率降低;温度一定时,烟气中SO2浓度升高,脱硫率降低.
(3)目前,科学家正在研究在一定条件下将乙烯(C2H4)和烟气混合除去二氧化硫,其反应
的过程可分为如下三步:
第一步:O2与Cu+反应生成Cu+(O2)
第二步:Cu+(O2)与SO2反应生成Cu+(SO3)2
第三步:Cu+(SO3)2与C2H4反应生成S、CO2、H2O和Cu+.
除去二氧化硫的总反应的化学方程式是2O2+SO2+C2H4$\frac{\underline{\;催化剂\;}}{\;}$S+2CO2+2H2O.

请回答下列问题:
(1)用熟石灰中和稀硫酸的化学方程式是Ca(OH)2+H2SO4═CaSO4+2H2O.
(2)为了研究脱硫率(脱硫率是已除去的二氧化硫的量占二氧化硫总量的百分比)与温度、烟气中SO2浓度的关系,他们进行了探究实验.实验结果如下:
| 实验序号 | 温度/℃ | 烟气中SO2浓度/10-2g•L-1 | 脱硫率/% |
| I | 25 | 2.5 | 99.5 |
| II | 25 | 3.2 | 97.1 |
| III | 40 | 2.5 | 94.3 |
(3)目前,科学家正在研究在一定条件下将乙烯(C2H4)和烟气混合除去二氧化硫,其反应
的过程可分为如下三步:
第一步:O2与Cu+反应生成Cu+(O2)
第二步:Cu+(O2)与SO2反应生成Cu+(SO3)2
第三步:Cu+(SO3)2与C2H4反应生成S、CO2、H2O和Cu+.
除去二氧化硫的总反应的化学方程式是2O2+SO2+C2H4$\frac{\underline{\;催化剂\;}}{\;}$S+2CO2+2H2O.
 A~I为初中化学常见的物质,它们之间存在如图所示关系,图中“→”表示转化关系,“-”表示能相互反应.已知A、B、C是氧化物,D、E、F是单质,G、H、I分别是碱、酸、盐,D是紫红色金属,H少量存在于胃液中.请回答:
A~I为初中化学常见的物质,它们之间存在如图所示关系,图中“→”表示转化关系,“-”表示能相互反应.已知A、B、C是氧化物,D、E、F是单质,G、H、I分别是碱、酸、盐,D是紫红色金属,H少量存在于胃液中.请回答:
 有一份铁粉与铜粉的混合物样品,为了解其组成,某同学用20克样品加入足量的稀硫酸中,待反应完全后过滤,称得不溶物质量为6克.试计算:
有一份铁粉与铜粉的混合物样品,为了解其组成,某同学用20克样品加入足量的稀硫酸中,待反应完全后过滤,称得不溶物质量为6克.试计算: