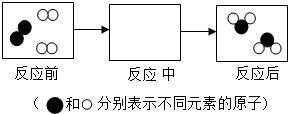
题目内容
15. 有一份铁粉与铜粉的混合物样品,为了解其组成,某同学用20克样品加入足量的稀硫酸中,待反应完全后过滤,称得不溶物质量为6克.试计算:
有一份铁粉与铜粉的混合物样品,为了解其组成,某同学用20克样品加入足量的稀硫酸中,待反应完全后过滤,称得不溶物质量为6克.试计算:(1)金属混合物中铁的质量分数.
(2)产生氢气的质量.
(3)在右图中画出产生氢气质量与参加反应的金属关系图象.
分析 由于铜排在了氢的后面所以不与酸反应,只有铁与硫酸反应,稀硫酸是足量的,所以不溶物为铜的质量,则铁的质量为20g-6g=14g,根据方程式列比例式进行计算,已知量是铁,即可求出氢气的质量.
解答 解:(1)由题意可知,铁的质量为:20g-6g=14g;
金属混合物中铁的质量分数为$\frac{14g}{20g}$×100%=70%
(2)设生成氢气的质量为x
Fe+H2SO4═FeSO4+H2↑
56 2
14g X
$\frac{56}{14g}$=$\frac{2}{x}$
x=0.5g
答:产生氢气的质量是0.5g
(3)根据计算结果,氢气质量与参加反应的金属关系图象为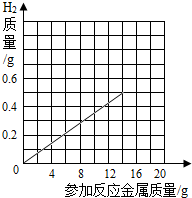
故答案为:(1)70%
(2)0.5g
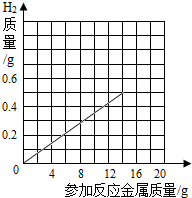
(3)
点评 解答本题的关键是要知道铜与硫酸不反应,因为铜排在了氢的后面,只有排在氢前面的金属才能与酸反应产生氢气.

练习册系列答案
相关题目
5.下列生活用品由有机合成材料制成的是( )
| A. | 塑料水盆 | B. | 不锈钢水龙头 | C. | 木桶 | D. | 纯棉毛巾 |
3. 化学反应也有“悄悄”进行的,小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.
化学反应也有“悄悄”进行的,小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.
探究一:二氧化碳是否与氢氧化钠发生了化学反应?
将二氧化碳通入盛有氢氧化钠溶液的大试管中(如图),取少量大试管中的液体与另一支试管中,滴加足量的稀盐酸,观察到有气泡产生,证明二氧化碳与氢氧化钠发生反应;
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】小明认为溶质是Na2CO3;小刚认为溶质是Na2CO3和NaOH
【查阅资料】CaCl2溶液呈中性
【实验验证】小刚为了验证自己的猜想,进行了如下实验,请你补充完整.
【实验反思】写出二氧化碳与氢氧化钠反应的化学方程式CO2+2NaOH=Na2CO3+H2O;
【实验拓展】同学们联想到了氢氧化钠与稀硫酸发生中和反应也观察不到明显现象,为了确定其反应是否发生,有同学设计了如下的实验方案:先用pH试纸测定氢氧化钠溶液的pH,
然后向其中滴加稀硫酸,边滴边测定混合溶液的pH.请你分析上述方案中,为什么要当测定pH值小于或等于7时才可以证明发生反应了,其原因是pH小于或等于7时,表明OH-被消耗,说明酸碱发生了反应.
【总结提高】试设计两种不同方案证明氢氧化钠和稀硫酸确实发生了反应,从实验操作、实验现象和实验结论等方面加以说明.
 化学反应也有“悄悄”进行的,小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.
化学反应也有“悄悄”进行的,小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.探究一:二氧化碳是否与氢氧化钠发生了化学反应?
将二氧化碳通入盛有氢氧化钠溶液的大试管中(如图),取少量大试管中的液体与另一支试管中,滴加足量的稀盐酸,观察到有气泡产生,证明二氧化碳与氢氧化钠发生反应;
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】小明认为溶质是Na2CO3;小刚认为溶质是Na2CO3和NaOH
【查阅资料】CaCl2溶液呈中性
【实验验证】小刚为了验证自己的猜想,进行了如下实验,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量大试管中的溶液于试管中,加入足量溶液,过滤;②向滤液滴加适量酚酞试液. | 酚酞试液变红 | 小刚猜想成立 |
【实验拓展】同学们联想到了氢氧化钠与稀硫酸发生中和反应也观察不到明显现象,为了确定其反应是否发生,有同学设计了如下的实验方案:先用pH试纸测定氢氧化钠溶液的pH,
然后向其中滴加稀硫酸,边滴边测定混合溶液的pH.请你分析上述方案中,为什么要当测定pH值小于或等于7时才可以证明发生反应了,其原因是pH小于或等于7时,表明OH-被消耗,说明酸碱发生了反应.
【总结提高】试设计两种不同方案证明氢氧化钠和稀硫酸确实发生了反应,从实验操作、实验现象和实验结论等方面加以说明.
| 实验操作 | 实验现象 | 实验结论 | |
方案一 | 氢氧化钠和稀硫酸发生了反应 | ||
方案二 |
20.下列物质属于纯净物的是( )
| A. | 医用酒精 | B. | 铁水 | C. | 洁净的空气 | D. | 稀有气体 |
7.2015年3月22日是第22届“世界水日”.联合国确定今年“世界水日”的宣传主题是“水与能源”.下列说法正确的是( )
| A. | 用明矾可以区别硬水和软水 | |
| B. | 为了防止水体污染,禁止使用农药和化肥 | |
| C. | 氢氧燃料电池可以将化学能直接转化为电能 | |
| D. | 石油经分馏或其他加工方法可以得到汽油、煤油等,这个过程是化学变化 |
5.下列实验现象的描述错误的是( )
| A. | 镁在空气中剧烈燃烧,发出耀眼的白光,生成白色固体 | |
| B. | 硫在氧气中燃烧产生二氧化硫 | |
| C. | 鸡蛋清溶液中加入浓硝酸,微热后,出现黄色沉淀 | |
| D. | 灼烧聚氯乙烯(PVC),可以闻到刺激性气味 |
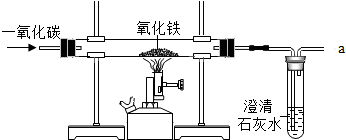 炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见如图.
炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见如图.