��Ŀ����
2���̷���FeSO4•7H2O�������ᷨ����̫�۵���Ҫ������������Ʊ�Fe2O3����ӡ��Fe3O4�ۡ���ԭ���۵ȣ����������̷�������һ��ʮ��������Ĺ�����ij�о���С��չ����ϵ���о������Ʊ�Fe2O3
������һ��
��1����ˮ����ͭ��ˮ�����ɫ������ͭ���壮
��2���̷���FeSO4•7H2O�����·ֽ����һ�ֽ���������ͼ�����̬�ǽ��������
��3��SO2����ɫ����Ϣ�Գ�ζ���ж����壬��ʹƷ����Һ��ɫ��
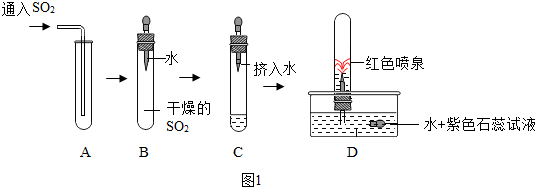
��ͬѧ������װ���Ʊ�Fe2O3����֤�̷����ȷֽ���������
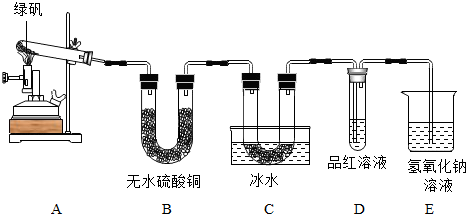
ʵ������з��֣�A���к���ɫ�������ɣ�B����ˮ����ͭ������C��U�ι�������ɫ���壨SO3��������D��Ʒ����Һ��ɫ��װ��E�����������ն�������ֹ��Ⱦ�������̷����·ֽ�Ļ�ѧ����ʽΪ2��FeSO4•7H2O��$\frac{\underline{\;����\;}}{\;}$Fe2O3+SO2��+SO3��+14H2O����
���Ʊ�Fe3O4
��ͬѧģ��������ӡ��Fe3O4�۵�ʵ���������£�
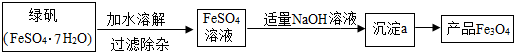
�����϶���Fe��OH��2��һ�ְ�ɫ������ˮ�Ĺ��壬�ڿ������ױ�������
FeSO4��Һ�м���NaOH��Һ����Ӧ�Ļ�ѧ����ʽ����Ϊ��FeSO4+2NaOH�TFe��OH��2��+Na2SO4����4Fe��OH��2+O2+2H2O�T4Fe��OH��3���ɳ���a���Fe3O4�Ļ�ѧ����ʽΪ��Fe��OH��2+2Fe��OH��3�TFe3O4+4H2O
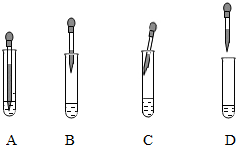
����ȡFe��OH��2����ȡ��ʵ������ǣ���ʢ��5mL����FeSO4��Һ���Թ��м���10��ֲ���ͣ�Ȼ���ý�ͷ�ιܼ���е�NaOH��Һ������O2������ͷ�ιܵ���ȷʹ�÷�����D������ĸ����
���Ʊ���ԭ����
�Ʊ���ԭ���۵Ĺ�ҵ�������£�
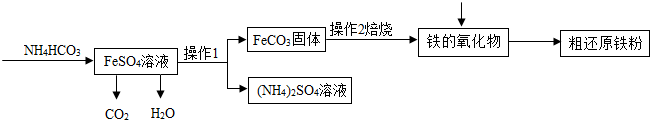
��1������1�������ǹ��ˣ�NH4HCO3��FeSO4��Һ��Ӧ�Ļ�ѧ����ʽΪFeSO4+2NH4HCO3=FeCO3��+��NH4��2SO4+CO2��+H2O��
��2������14.06g�ֻ�ԭ���ۣ�����ֻ�ԭ���������ʽ�������FexC��������������ȫ��Ӧ���õ�0.22g
CO2������ͬ�����Ĵֻ�ԭ����������ϡ���ᷴӦ���õ�0.48gH2��FexC��ϡ���ᷴӦ������H2������ͨ������ȷ��FexC�Ļ�ѧʽ����д��������̣�Fe2C��
��3���ֻ�ԭ���۾��ӹ��������ɴ���ԭ���ۣ�����ԭ���ۺ�ˮ�����ڸ���������Ҳ���Ƶ�������������ͬʱ����һ�����壮��װ����ͼ��ʾ��
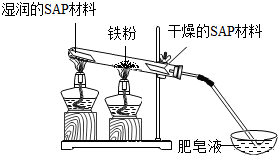
SAP������ˮ��ǿ��ʪ���SAP������Ϊ�÷�Ӧ�����ṩˮ������ʵ�鿪ʼһ��ʱ��۲쵽�ڷ���Һ���д��������ݲ������������û���ܵ�ȼ��ͬʱ�з�����Ʈ�����У����ɵ������������������SAP���������Ǹ������
���� �������⣬�̷���FeSO4•7H2O�����·ֽ����һ�ֽ���������ͼ�����̬�ǽ����������ˮ����ͭ��ˮ�����ɫ������ͭ���壬SO2����ɫ����Ϣ�Գ�ζ���ж����壬��ʹƷ����Һ��ɫ�����з������
��� �⣺������һ���̷���FeSO4•7H2O�����·ֽ����һ�ֽ���������ͼ�����̬�ǽ�������������⣬���������������ʻ�۲쵽A���к���ɫ�������ɣ�
�ᾧˮ����ʧȥ�ᾧˮ��ˮ���ɣ���ˮ����ͭ��ˮ�����ɫ������ͭ���壬��B����ˮ����ͭ������C��U�ι�������ɫ���壨SO3��������D��Ʒ����Һ��ɫ��˵���ж��������������ɣ�SO2����ɫ����Ϣ�Գ�ζ���ж����壬��װ��E�����������ն�������ֹ��Ⱦ������
�̷����·ֽ�Ļ�ѧ����ʽΪ2��FeSO4•7H2O��$\frac{\underline{\;����\;}}{\;}$Fe2O3+SO2��+SO3��+14H2O����
�����϶���
��FeSO4��Һ�м���NaOH��Һ�ᷢ����Ӧ��FeSO4+2NaOH�TFe��OH��2��+Na2SO4�����ɰ�ɫ��Fe��OH��2��������ɫ��Fe��OH��2 ���ױ�������������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ��Fe��OH��3����Ӧ��4 Fe��OH��2+O2 +2H2O�T4 Fe��OH��3��
����ȡFe��OH��2����ȡ��ʵ������ǣ���ʢ��5mL����FeSO4��Һ���Թ��м���10��ֲ���ͣ�Ȼ���ý�ͷ�ιܼ���е�NaOH��Һ������O2������ͷ�ιܵ���ȷʹ�÷�����A��
���Ʊ���ԭ����
��1������1�������ǹ��ˣ�����������̼����立�Ӧ����̼����������李�ˮ�Ͷ�����̼����ѧ����ʽΪ��FeSO4+2NH4HCO3=FeCO3��+��NH4��2SO4+CO2��+H2O��
��2������14.06g��ԭ���ۣ�������FexC�����������м��ȣ��õ�0.22gCO2��̼Ԫ�ص�����=0.22g��$\frac{12}{44}$=0.06g
����ͬ�����Ļ�ԭ�������������ᷴӦ���õ�0.48gH2�����ݷ�Ӧ����ʽ���㣺��������������Ϊx
Fe+H2SO4=FeSO4+H2����
56 2
x 0.48g
$\frac{56}{2}$=$\frac{x}{0.48g}$
x=13.44g
FexC������=14.06g-13.44g=0.62g��
FexC������Ԫ�ص�����=0.62g-0.06g=0.56g
��56x��12=0.56g��0.06g
x=2
���Ի�ѧʽΪFe2C��
��3��SAP������ˮ��ǿ��ʪ���SAP������Ϊ�÷�Ӧ�����ṩˮ������ʵ�鿪ʼһ��ʱ��۲쵽�ڷ���Һ���д��������ݲ������������û���ܵ�ȼ��ͬʱ�з�����Ʈ�����У����ɵ������������������SAP���������Ǹ�������ã�
�ʴ�Ϊ��
������һ�����أ����ն�������ֹ��Ⱦ������2��FeSO4•7H2O��$\frac{\underline{\;����\;}}{\;}$Fe2O3+SO2��+SO3��+14H2O����
�����϶���FeSO4+2NaOH�TFe��OH��2��+Na2SO4��D��
���Ʊ���ԭ����
��1�����ˣ�FeSO4+2NH4HCO3=FeCO3��+��NH4��2SO4+CO2��+H2O��
��2��Fe2C��
��3����������������ã�
���� ������һ���Ѷȣ�������Ŀ������Ϣ�����������ѧ֪ʶ����������ļ�������ӷ�������ѧ����ʽ����д�����ȣ�����ȷ�����Ĺؼ���

̽��һ��SO2����ȡ
��1��ʵ���ҳ��ù����������ƣ�Na2SO3����ϡ�����ڳ����·�Ӧ��ȡ��������ѡ����װ����ҪӦ�ÿ��ǵ�������A��B������ţ��ɶ�ѡ����
A����Ӧ���״̬ B����Ӧ���� C�������ܶ� D�������ܽ���
��2��̽�������������ʣ�����ȤС���������ͼ1��ʾ��ʵ�飮
ͨ������ʵ�飬���Ʋ�SO2����������У�
��SO2�ܶȱȿ�����
��SO2������ˮ�Ⱥ����𰸣�
̽������CO2��SO2���ʵıȽ�
��ȤС����Ʋ�������ͼ2ʵ�飬̽���Ƚ�CO2��SO2�Ļ�ѧ���ʣ�
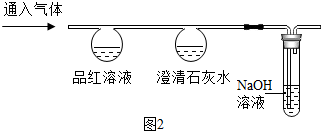
| ʵ��� | ʵ��� | |
| ͨ��CO2 | ͨ��SO2 | |
| Ʒ����Һ | �����Ա仯 | ��ɫ��Ϊ��ɫ |
| ����ʯ��ˮ | ��ɫ���� | ��ɫ���� |
�ٶ��������������ʯ��ˮ��Ӧ������������ƣ�CaSO3����ˮ��д���÷�Ӧ�Ļ�ѧ����ʽSO2+Ca��OH��2=CaSO3��+H2O��
�ڼ���CO2��SO2�ķ����ǽ�����ֱ�ͨ��Ʒ����Һ����ɫ��ȥ��SO2�������Ա仯����CO2��ʵ�����NaOH��Һ������������β������ֹ������β������ֹ����Ⱦ������
̽�������ⶨ������SO2�ĺ�����̽��С���������ʵ��
���������ϡ��ٵ�ˮ�����۱���ɫ��
�ڶ����������ˮ��Ӧ�Ļ�ѧ����ʽΪ��SO2+I2+2H2O=H2SO4+2HI
��SO2��I2����Է��������ֱ�Ϊ��64��254����
���ҹ����������������ж�ÿ�ο��������ⶨ��SO2���Ũ����ֵ
| SO2���Ũ����ֵ����λmg/m3�� | ||
| һ���� | ������ | ������ |
| 0.15 | 0.50 | 0.70 |
���װ�õ������ԣ�
�����Թ��м���1g������������Ϊ0.0127%�ĵ�ˮ��������������ˮϡ�ͣ��ٵ���2-3�ε�����Һ�����Ƴ�ϡ��Һ��
����ָ���ص���ע������ȡ����140��ע�������Թ��У�����ÿ�γ���500mL��
��ʵ���֪��
�ٵ���Һ����ɫ�����ɫʱ��Ӧǡ����ȫ��
���ɴ˿ɼ��������SO2�ĺ���0.46mg/m3�������ȷ��0.01��������ص�Ŀ�����SO2�ĺ������ڶ����������ϱ������оٵĵȼ�����
| A�� | CO2��CO��-��ȼ | |
| B�� | KNO3��NaCl��-���½ᾧ | |
| C�� | NaCl��Һ��Na2SO4��-����������BaCl2��Һ������ | |
| D�� | ZnSO4��Һ��CuSO4��-���������п�ۣ����� |
| A�� | ��ȼ�ŵ�ľ������O2��CO2��N2�������� | |
| B�� | ��ˮ����CuS04��NaOH��NH4NO3���ֹ��� | |
| C�� | �����յķ�������ľ̿�ۡ�CuO��Fe3O4���ֺ�ɫ��δ | |
| D�� | �÷�̪��Һһ���Լ���H2SO4��KOH��NaCl������Һ |
| A�� | ���� | B�� | ʳ��ˮ | C�� | ����ʯ | D�� | ���� |
| �¶�/�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| �ܽ��/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
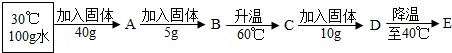
��ҺD�Dz����ͣ�����͡������͡�����Һ����ҺE����������9.2g��
�ڽ�ʢ����ҺE��С�ձ�����ʢ��ˮ�Ĵ��ձ��У�����ձ��ڼ���NaOH���壬С�ձ��ڵĹ����ܽ⣬ԭ�����������ƹ�������ˮ���ȣ�ʹ���Ȼ�淋��ܽ��������ܽ⣮
 ��֪Mg����CO2��ȼ������̼��һ�ְ�ɫ�������ʣ�ij��ѧ��ȤС������ͼ��ʾװ���Ʊ�CO2����Mg��CO2��ȼ�����ɵİ�ɫ�������ʽ���̽����
��֪Mg����CO2��ȼ������̼��һ�ְ�ɫ�������ʣ�ij��ѧ��ȤС������ͼ��ʾװ���Ʊ�CO2����Mg��CO2��ȼ�����ɵİ�ɫ�������ʽ���̽����