题目内容
14.对四种无色溶液进行离子检验,检验结果如下,其中明显不正确的是( )| A. | SO42- OH- Cl- K+ | B. | Na+ NO3- OH- Cl- | ||
| C. | K+ Na+ NO3- Cl- | D. | K+ CO32- H+ Ba2+ |
分析 利用所给的离子之间不能结合生成水、气体、沉淀能够共存,且注意带色的离子条件的限制.
解答 解:A、四种离子不能结合生成水、气体、沉淀,能大量共存,且不存在带色的离子,故选项错误;
B、四种离子不能结合生成水、气体、沉淀,能大量共存,且不存在带色的离子,故选项错误;
C、四种离子不能结合生成水、气体、沉淀,能大量共存,且不存在带色的离子,故选项错误;
D、碳酸根离子和氢离子结合产生水和二氧化碳,和钡离子结合产生碳酸钡沉淀,不能共存,因此检测结果错误,故选项正确;
故选项为:D.
点评 本题考查离子的共存问题,学生能利用复分解反应发生的条件来解答即可,还应注意隐含信息的挖掘.

练习册系列答案
相关题目
2. 现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.
现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.
(1)下列方法能检查该装置气密性的是AB.
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)过氧化氢分解的文字表达式是过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,二氧化锰起催化 作用.
(3)甲小组有如下实验设计方案,完成下表.
(4)实验结论:浓度越大,过氧化氢分解速率越快.表格中温度、催化剂、浓度三个变量只有浓度这个变量不同,这种探究实验的方法叫控制变量法.
 现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.
现甲、乙两化学小组安装两套如下相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素.(1)下列方法能检查该装置气密性的是AB.
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差.
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差.
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差.
(2)过氧化氢分解的文字表达式是过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,二氧化锰起催化 作用.
(3)甲小组有如下实验设计方案,完成下表.
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 | 现象 |
| 甲组实验Ⅰ | 探究浓度对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2 | 反应较缓和 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 | 剧烈反应 |
6.正确的实验操作对实验结果、人身安全非常重要. 下列操作正确的是( )
| A. |  验满氧气 | B. |  倾倒液体 | C. |  读取液体体积 | D. |  点燃酒精灯 |
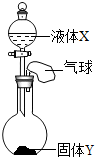 如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀.如表中液体X和固体Y的组合,不符合题意的是( )
如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀.如表中液体X和固体Y的组合,不符合题意的是( )