题目内容
15.硫化氢(H2S)是一种具有臭鸡蛋气味的致命毒气,它的密度比空气大,可溶于水形成氢硫酸,氢硫酸具有酸的通性.实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,同时生成FeSO4.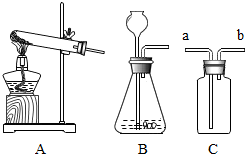
(1)在图中,应选用图B作为制取H2S的装置.
(2)收集H2S气体满后,对产生尾气的处理方法是:通入水中或碱溶液中.
(3)请写出硫化亚铁和稀硫酸反应的化学方程式FeS+H2SO4=FeSO4+H2S↑.
分析 制取装置包括加热和不需加热两种,实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,同时生成FeSO4,因此不需要加热;硫化氢可溶于水形成氢硫酸,氢硫酸具有酸的通性,因此收集H2S气体满后,对产生尾气的处理方法是:通入水中或碱溶液中.
解答 解:(1)实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,因此不需要加热;故答案为:B;
(2)收集H2S气体满后,对产生尾气的处理方法是:通入水中或碱溶液中;故答案为:通入水中或碱溶液中;
(3)硫化亚铁和稀硫酸反应生成H2S,同时生成FeSO4,故答案为:FeS+H2SO4=FeSO4+H2S↑;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和尾气的处理等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
5.如图所示的溶解度曲线,下列说法中不正确的是( )


| A. | 图中a点表示t2℃时100g水中最多溶解甲物质25g | |
| B. | t1℃时,甲、乙两物质的饱和溶液中含溶质的质量相等 | |
| C. | 甲物质的溶解度随温度的升高而增大 | |
| D. | t1℃时,甲、乙两物质的饱和溶液中溶质质量分数相等 |
6.下列有关溶液的叙述正确的是 ( )
| A. | 无色、透明的液体一定是溶液 | |
| B. | 溶质的溶解度都随温度的升高而增大 | |
| C. | 饱和溶液就是不能再溶解任何物质的溶液 | |
| D. | 饱和溶液和不饱和溶液在一定条件下可以互相转化 |
20.熟石灰是一种常见的化学药品,下列关于熟石灰的说法错误的是( )
| A. | 熟石灰可以用作建筑材料是因为它与空气中的二氧化碳气体反应生成了不溶于水的碳酸钙 | |
| B. | 杭州富阳制造宣纸常用熟石灰制浆,这是因为熟石灰具有腐蚀性 | |
| C. | 冬季往往定期向道路两旁的树干上刷上石灰水,是因为氢氧离子有一定的杀菌作用 | |
| D. | 熟石灰可以用来检验二氧化碳等酸性气体 |
7.下列符号能同时表示一种元素,又能表示一个原子,还能表示一种单质的是( )
| A. | H | B. | CO2 | C. | Fe | D. | O2 |
20.下列现象中,属于化学变化的是( )
| A. | 樟脑丸放在衣橱中逐渐消失 | B. | 木材做成课桌 | ||
| C. | 食物腐败 | D. | 石蜡熔化 |
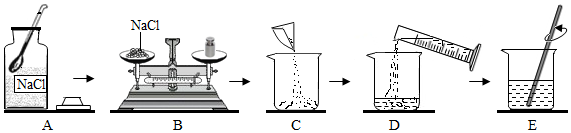
 图为精制粗盐的示意图,回答:
图为精制粗盐的示意图,回答: 为研究CO2与NaOH固体的反应,某同学设计了如图实验.
为研究CO2与NaOH固体的反应,某同学设计了如图实验.