题目内容
4.如图是配置50g质量分数为5%的氯化钠溶液的操作过程示意图:试回答: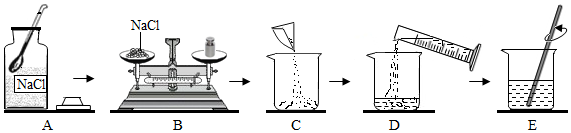
(1)D操作应选用50mL 的量筒(从10mL、50mL、100mL中选择);
(2)E操作的作用是搅拌,加快氯化钠的溶解速度.
(3)如果配制过程中出现以下情况可能造成对所配溶液的溶质质量分数的误差(填“偏高”、“偏低”、“无影响”):
A、所用氯化钠药品不纯偏低;
B、量取水时俯视读数偏高;
C、配制完后将溶液转移至试剂瓶时洒出了一些无影响.
分析 (1)根据量筒使用时的就近原则进行分析;
(2)根据玻璃棒搅拌的作用是加速溶解进行分析;
(3)根据溶质的质量分数=$\frac{溶质的质量}{溶液的质量}$×100%,以及操作所引起的溶质和溶剂的质量变化进行分析.
解答 解:(1)需要水的质量是50g-2.5g=47.5g,水的密度是1g/cm3,故量取水的体积是47.5mL,所以应选择50mL的量筒;
(2)玻璃棒在溶解过程中的作用是加速固体溶解;
(3)A、所用氯化钠药品不纯,则实际氯化钠的质量小于2.5g,使用所配溶液溶质的质量分数偏低;
B、量取水时俯视读数,读数偏大,实际量取液体的体积小于47.5mL,使用溶质的质量分数偏高;
C、溶液具有均一性,配制完后将溶液转移至试剂瓶时洒出了一些,溶质的质量分数不变;
故答案为:(1)50;
(2)搅拌,加快氯化钠的溶解速度;
(3)A、偏低;
B、偏高;
C、无影响.
点评 本题难度不大,明确一定溶质质量分数溶液的配制的步骤(计算、称量、溶解)、注意事项等是正确解答此类题的关键.

练习册系列答案
相关题目
12.在电解水的实验中可以直接观察到的实验现象是( )
| A. | 水是由氢、氧两种元素组成的 | |
| B. | 每个水分子是由两个氢原子和一个氧原子构成的 | |
| C. | 在电极上均有气泡产生,两个玻璃管内气体的体积比约为2:1 | |
| D. | 有氢气和氧气产生,且体积比为2:1 |
19.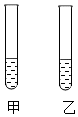 某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象.则下列分析正确的是( )
某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象.则下列分析正确的是( )
 某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象.则下列分析正确的是( )
某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象.则下列分析正确的是( )| A. | 甲试管中固体全部溶解,说明甲试管中的溶液为稀溶液 | |
| B. | 乙试管底部有固体,说明乙试管中的溶液为浓溶液 | |
| C. | 此时蔗糖溶液肯定未饱和,而熟石灰溶液一定已饱和 | |
| D. | 该实验现象说明该温度下蔗糖的溶解度比熟石灰大 |
9.某温度下,向盛有200克蔗糖溶液的烧杯中再加入10克蔗糖,充分搅拌后,一定保持不变的是( )
| A. | 溶质的质量 | B. | 溶液的质量 | C. | 溶质的质量分数 | D. | 该溶质的溶解度 |
16.下列物之间的转化,能通过一步反应实现的是( )
①CaCO3→CO2 ②CaO→Ca(OH)2 ③H2O2→H2O ④HCl→HNO3 ⑤Fe→FeCl3.
①CaCO3→CO2 ②CaO→Ca(OH)2 ③H2O2→H2O ④HCl→HNO3 ⑤Fe→FeCl3.
| A. | ①②③④ | B. | ①②③⑤ | C. | ①③④⑤ | D. | ②③④⑤ |
8.同学们在学习金属与盐溶液的反应时,老师强调:“金属K、Ca、Na必须除外”,化学兴趣小组的同学们对此产生了兴趣,并在老师的指导下,进行如下探究:
【提出问题】将金属钠没入到硫酸铜溶液中,结果会怎样?
【查找资料】
(1)少量钠通常保存在煤油中;
(2)钠是银白色的软金属,可用小刀切割,熔点97.81℃,沸点882.9℃,密度为0.97g/cm3.
【做出猜想】猜想Ⅰ:放出气体,生成蓝色沉淀,能置换出铜.
猜想Ⅱ:放出气体,生成蓝色沉淀,不能置换出铜.
【实验探究】
【现象分析】
(1)钠熔成小球是因为反应放热,温度达到钠的熔点;
(2)钠球游动,发出“嘶嘶”声响说明有气体产生;
(3)析出蓝色沉淀是因为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓(用化学方程式表示).
【继续探究】有部分同学认为置换出的铜可能被蓝色沉淀掩盖,于是他们进一步探究:
【实验结论】在金属活动性顺序里,位于前面的金属(K、Ca、Na必须除外)能把位于后面的金属从它们盐的溶液里置换出来.
【提出问题】将金属钠没入到硫酸铜溶液中,结果会怎样?
【查找资料】
(1)少量钠通常保存在煤油中;
(2)钠是银白色的软金属,可用小刀切割,熔点97.81℃,沸点882.9℃,密度为0.97g/cm3.
【做出猜想】猜想Ⅰ:放出气体,生成蓝色沉淀,能置换出铜.
猜想Ⅱ:放出气体,生成蓝色沉淀,不能置换出铜.
【实验探究】
| 实验操作 | 实验现象 |
| ①取10mL一定溶质质量分数的硫酸铜溶液,倒入50mL的烧杯里 ②取一块钠,用滤纸吸干表面煤油,再切取绿豆大小的一块,投入溶液中 | 钠浮在液面上,熔化成闪亮小球,钠球游动,发出“嘶嘶”的声响,析出蓝色沉淀 |
(1)钠熔成小球是因为反应放热,温度达到钠的熔点;
(2)钠球游动,发出“嘶嘶”声响说明有气体产生;
(3)析出蓝色沉淀是因为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓(用化学方程式表示).
【继续探究】有部分同学认为置换出的铜可能被蓝色沉淀掩盖,于是他们进一步探究:
| 实验操作 | 实验现象 | 结论 |
| 取烧杯中少许沉淀于试管中,再向其中加入过量的稀硫酸 | 沉淀全部溶解,溶液变蓝色 | ①反应的化学方程式为Cu(OH)2+H2SO4═CuSO4+2H2O ②沉淀中不含铜,原因是沉淀全部溶解 |
9.用焊锡焊接铁时,在焊接处先滴几滴盐酸的目的是( )
| A. | 除去铁锈 | B. | 清洗焊条 | C. | 除去泥沙 | D. | 氧化焊条 |