题目内容
18.如图是实验室常用的气体制备、收集的多种功能装置.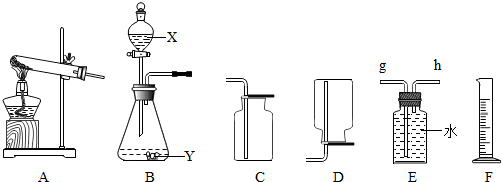
①若实验室用A装置加热氯酸钾和二氧化锰混合物制取氧气,其化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
②B装置中X装置的名称为分液漏斗;若B装置X中盛放稀盐酸、Y中盛放石灰石,B与C组成发生、收集CO2气体的系列装置,检验CO2收满的方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.检验制得气体是否为二氧化碳的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
③若实验室用锌粒和稀硫酸制取氢气,可选择的发生装置为B,发生的化学方程式为Zn+H2SO4=ZnSO4+H2↑.若用排水法收集并测定氢气的体积,氢气从E装置导管口h(填“g”或“h”)进.选用仪器F测量排出水的体积,仪器F的名称是量筒.
④对锌与稀硫酸反应快慢的影响因素进行探究.反应过程中,利用前10min内收集的氢气体积比较反应的快慢,控制其他条件相同,进行如图四组实验,获得数据如表:
| 实验编号 | 试剂 | 前10min内产生的氢气体积/(mL) | |
| 不同纯度的锌 | 不同体积和溶质质量分数的稀硫酸 | ||
| a | 纯锌 | 30mL30% | 564.3 |
| b | 含杂质的锌 | 30mL30% | 634.7 |
| c | 纯锌 | 30mL20% | 449.3 |
| d | 纯锌 | 40mL30% | 602.8 |
分析 分液漏斗可以控制反应的速度,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.由表格信息可知:要比较不同溶质质量分数的硫酸对反应快慢的影响,应选择的实验编号是a和c;可以得出的结论是:在其它条件相同的情况下,稀硫酸的溶质质量分数越大,反应速度越快.
解答 解:(1)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)分液漏斗可以控制反应的速度,二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;故答案为:分液漏斗;将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;CO2+Ca(OH)2=CaCO3↓+H2O;
(3)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;若用排水法收集并测定氢气的体积,氢气从E装置导管口h进,选用仪器F测量排出水的体积,仪器F的名称是量筒,故答案为:B;Zn+H2SO4=ZnSO4+H2↑;h;量筒;
(4)由表格信息可知:要比较不同溶质质量分数的硫酸对反应快慢的影响,应选择的实验编号是a和c;可以得出的结论是:在其它条件相同的情况下,稀硫酸的溶质质量分数越大,反应速度越快;故答案为:a和c;在其它条件相同的情况下,稀硫酸的溶质质量分数越大,反应速度越快;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的检验和验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. |  米饭 | B. |  西红柿 | C. |  牛肉 | D. |  花生油 |

(1)甲组同学取少量的氢氧化钠溶液于烧杯中,用酸度计测得该溶液的pH同时插入一支温度计,测量溶液的温度(如图1示).用胶头滴管吸取稀盐酸,逐滴加入盛有氢氧化钠溶液的烧杯中,边滴加边搅拌.此时可观察到的现象是:酸度计上显示的数据逐渐减少(选填“增大”、“减少”或“不变”),温度计上显示的数据逐渐升高,由此可知,酸和碱的中和反应属于放热(选填“吸热”或“放热”)反应.
(2)乙组的同学改用固体氢氧化钠与稀盐酸反应来探究中和反应中能量的变化情况,你认为该方案不合理(选填“合理”或“不合理”),原因固体氢氧化钠溶于水会放出热量.
(3)丙组同学用另外一瓶氢氧化钠溶液进行实验时,当往烧杯中滴加稀盐酸时,发现有少量的气泡冒出,小组同学根据这一现象进行讨论,一致认为其原因可能是氢氧化钠溶液已经变质,原因是CO2+2NaOH═Na2CO3+H2O(写化学方程式)
(4)丁组同学借助酚酞试液来判断氢氧化钠溶液与稀盐酸发生中和反应时,在烧杯中加入氢氧化钠溶液后,滴几滴酚酞溶液,然后加入一定量稀盐酸,最后溶液为无色.小金认为溶液显中性.小东认为不一定.小东同学设计以下实验进行了验证,结果否定小金的结论:
| 实验步骤 | 实验现象 | 结论 |
| 取少量反应后的溶液于试管中,滴加几滴紫色的石蕊试液 | 石蕊试液变红色 | 没有完全中和 |
| A. | 木炭在氧气中燃烧,发出白色火焰 | |
| B. | 红磷在氧气中燃烧产生白雾,放出大量的热 | |
| C. | 硫在氧气中燃烧发出淡蓝色火焰,放热,生成有刺激性气味的气体 | |
| D. | 木炭燃烧生成二氧化碳,倒入瓶中的澄清石灰水变浑浊 | |
| E. | 铁丝在氧气中燃烧火星四射,放热,生成黑色物质 |
(1)管道煤气的主要成分是CO和少量碳氢化合物,天然气的主要成分是CH4,它们的燃烧反应如下:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
已知在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子,试根据以上方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是天然气,因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进的方法是增大进气口(填“增大”或“减小”),如不加改进可能产生的不良后果是有毒的CO生成,甚至有固体残留物堵塞燃气管道.
(2)液化石油气的主要成分是丙烷(C3H8)、丁烷(C4H10)等,它们的某些性质见下表:
| 乙烷(C2H6) | 丙烷(C3H8) | 丁烷(C4H10) | |
| 熔点(℃) | -183.3 | -189.7 | -138.4 |
| 沸点(℃) | -88.6 | -42.1 | -0.5 |
有趣的是,使用液化石油气的居民在改用天然气时,也将涉及灶具的调整,已知碳氢化合物充分燃烧的产物跟甲烷相同,请根据液化石油气的燃烧方程式,说明灶具改进的方法:将进气口增大.

