题目内容
1.化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:
(1)甲组同学取少量的氢氧化钠溶液于烧杯中,用酸度计测得该溶液的pH同时插入一支温度计,测量溶液的温度(如图1示).用胶头滴管吸取稀盐酸,逐滴加入盛有氢氧化钠溶液的烧杯中,边滴加边搅拌.此时可观察到的现象是:酸度计上显示的数据逐渐减少(选填“增大”、“减少”或“不变”),温度计上显示的数据逐渐升高,由此可知,酸和碱的中和反应属于放热(选填“吸热”或“放热”)反应.
(2)乙组的同学改用固体氢氧化钠与稀盐酸反应来探究中和反应中能量的变化情况,你认为该方案不合理(选填“合理”或“不合理”),原因固体氢氧化钠溶于水会放出热量.
(3)丙组同学用另外一瓶氢氧化钠溶液进行实验时,当往烧杯中滴加稀盐酸时,发现有少量的气泡冒出,小组同学根据这一现象进行讨论,一致认为其原因可能是氢氧化钠溶液已经变质,原因是CO2+2NaOH═Na2CO3+H2O(写化学方程式)
(4)丁组同学借助酚酞试液来判断氢氧化钠溶液与稀盐酸发生中和反应时,在烧杯中加入氢氧化钠溶液后,滴几滴酚酞溶液,然后加入一定量稀盐酸,最后溶液为无色.小金认为溶液显中性.小东认为不一定.小东同学设计以下实验进行了验证,结果否定小金的结论:
| 实验步骤 | 实验现象 | 结论 |
| 取少量反应后的溶液于试管中,滴加几滴紫色的石蕊试液 | 石蕊试液变红色 | 没有完全中和 |
分析 (1)由于中和反应是放热反应,所以会使溶液的温度升高,
(2)根据氢氧化钠固体溶解放热来分析;
(3)二氧化碳容易与氢氧化钠反应生成碳酸钠;
(4)首先判断该实验的推论不正确,并找出理由,进而提出可行的实验方案,以及实验现象、结论;
(5)根据NaOH和HCl反应的化学方程式,用氢氧化钠溶液中溶质NaOH的量可求出废液中溶质HCl的量和生成氯化钠的质量,进而求出废液中HCl的质量分数.
解答 解:(1)用胶头滴管吸取稀盐酸,逐滴加入盛有氢氧化钠溶液的烧杯中,边滴加边搅拌.此时可观察到的现象是:酸度计上显示的数据逐渐减少,温度计上显示的数据逐渐升高,由此可知,酸和碱的中和反应属于放热反应;
(2)氢氧化钠固体溶于水会放出热量,无法判断是否是二者发生中和反应放热,故填:不合理;固体氢氧化钠溶于水会放出热量;
(3)氢氧化钠能与二氧化碳反应生成碳酸钠而变质,应该密封保存,故填:CO2+2NaOH═Na2CO3+H2O;
(4)由于酚酞遇到酸性或中性溶液都不变色,因此酚酞呈无色时并能说明溶液呈中性,探究两物质是否恰好完全反应,只要证明盐酸是否存在即可;故答案为:
| 实验步骤 | 实验现象 | 结论 |
| 取少量反应后的溶液于试管中,滴加几滴紫色的石蕊试液 | 石蕊试液变红色 | 没有完全中和 |
| 取少量反应后的溶液于试管中,加入锌(或石灰石) | 有气泡冒出 | 没有完全中和 |
20g氢氧化钠溶液中含溶质NaOH的质量为20g×20%=4g
NaOH+HCl=NaCl+H2O
40 36.5
4g x
$\frac{40}{36.5}=\frac{4g}{x}$
x=3.65g
废水中盐酸的溶质质量分数为:$\frac{3.65g}{50g}$×100%=7.3%
答:废水中盐酸的溶质质量分数为7.3%.
点评 结合课本知识和实验技能,考查了学生的分析问题,解决问题的能力;此题综合性较强,考查出学生将理论知识与实验相结合的能力,还考查学生的创新能力,是一道不错的综合题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.如图是实验室常用的气体制备、收集的多种功能装置.
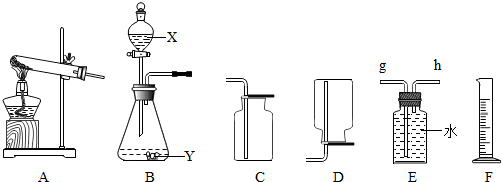
①若实验室用A装置加热氯酸钾和二氧化锰混合物制取氧气,其化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
②B装置中X装置的名称为分液漏斗;若B装置X中盛放稀盐酸、Y中盛放石灰石,B与C组成发生、收集CO2气体的系列装置,检验CO2收满的方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.检验制得气体是否为二氧化碳的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
③若实验室用锌粒和稀硫酸制取氢气,可选择的发生装置为B,发生的化学方程式为Zn+H2SO4=ZnSO4+H2↑.若用排水法收集并测定氢气的体积,氢气从E装置导管口h(填“g”或“h”)进.选用仪器F测量排出水的体积,仪器F的名称是量筒.
④对锌与稀硫酸反应快慢的影响因素进行探究.反应过程中,利用前10min内收集的氢气体积比较反应的快慢,控制其他条件相同,进行如图四组实验,获得数据如表:
要比较不同溶质质量分数的硫酸对反应快慢的影响,应选择的实验编号是a和c;可以得出的结论是:在其它条件相同的情况下,稀硫酸的溶质质量分数越大,反应速度越快.

①若实验室用A装置加热氯酸钾和二氧化锰混合物制取氧气,其化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
②B装置中X装置的名称为分液漏斗;若B装置X中盛放稀盐酸、Y中盛放石灰石,B与C组成发生、收集CO2气体的系列装置,检验CO2收满的方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.检验制得气体是否为二氧化碳的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
③若实验室用锌粒和稀硫酸制取氢气,可选择的发生装置为B,发生的化学方程式为Zn+H2SO4=ZnSO4+H2↑.若用排水法收集并测定氢气的体积,氢气从E装置导管口h(填“g”或“h”)进.选用仪器F测量排出水的体积,仪器F的名称是量筒.
④对锌与稀硫酸反应快慢的影响因素进行探究.反应过程中,利用前10min内收集的氢气体积比较反应的快慢,控制其他条件相同,进行如图四组实验,获得数据如表:
| 实验编号 | 试剂 | 前10min内产生的氢气体积/(mL) | |
| 不同纯度的锌 | 不同体积和溶质质量分数的稀硫酸 | ||
| a | 纯锌 | 30mL30% | 564.3 |
| b | 含杂质的锌 | 30mL30% | 634.7 |
| c | 纯锌 | 30mL20% | 449.3 |
| d | 纯锌 | 40mL30% | 602.8 |


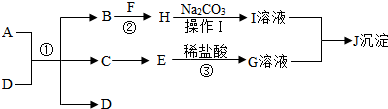 下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,如图是它们之间的转化关系,请回答:
下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,如图是它们之间的转化关系,请回答:
 小明和小红对市场上销售的一种真空充气包装的形如小枕头“蛋黄派”发生了兴趣,如图所示.他们查阅资料获知:这种真空充气包装技术,即将食品装入包装袋,抽出包装袋内空气,再充入某种气体,然后封口.它能使食品保持原有的色、香、味及营养价值,防止食品受压而破碎变形.那么,这是什么气体呢?小红猜想是氮气,小明猜想是二氧化碳.
小明和小红对市场上销售的一种真空充气包装的形如小枕头“蛋黄派”发生了兴趣,如图所示.他们查阅资料获知:这种真空充气包装技术,即将食品装入包装袋,抽出包装袋内空气,再充入某种气体,然后封口.它能使食品保持原有的色、香、味及营养价值,防止食品受压而破碎变形.那么,这是什么气体呢?小红猜想是氮气,小明猜想是二氧化碳.