题目内容
13.目前城市居民所使用的燃料主要是管道煤气或液化石油气,随着西东输工程的输气管道已经铺设到浙江省境内,我省居民将陆续使用天然气作为民用燃料.(1)管道煤气的主要成分是CO和少量碳氢化合物,天然气的主要成分是CH4,它们的燃烧反应如下:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
已知在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子,试根据以上方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是天然气,因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进的方法是增大进气口(填“增大”或“减小”),如不加改进可能产生的不良后果是有毒的CO生成,甚至有固体残留物堵塞燃气管道.
(2)液化石油气的主要成分是丙烷(C3H8)、丁烷(C4H10)等,它们的某些性质见下表:
| 乙烷(C2H6) | 丙烷(C3H8) | 丁烷(C4H10) | |
| 熔点(℃) | -183.3 | -189.7 | -138.4 |
| 沸点(℃) | -88.6 | -42.1 | -0.5 |
有趣的是,使用液化石油气的居民在改用天然气时,也将涉及灶具的调整,已知碳氢化合物充分燃烧的产物跟甲烷相同,请根据液化石油气的燃烧方程式,说明灶具改进的方法:将进气口增大.
分析 (1)根据化学方程式中的微观粒子个数比进行分析消耗氧气的多少;由于燃烧同样质量的天然气和一氧化碳,天然气燃烧需要的氧气多,燃烧管道煤气的灶具如需改烧天然气,需要加大氧气的量;根据燃料不完全燃烧时生成一氧化碳,容易生成污染大气进行解答;
(2)根据冬天温度低丁烷的沸点高不易气化分析,根据燃烧需要的氧气的量分析灶具调整的具体措施.
解答 解:(1)由化学方程式的微观粒子个数比可知,燃烧相同体积的管道煤气和天然气时,天然气消耗的氧气多;燃烧管道煤气的灶具如需改燃天然气,灶具的改进方法是增大进风口;如果燃料不完全燃烧,会有毒的CO生成,甚至有固体残留物堵塞燃气管道;
(2)由表中的数据可知,冬天使用液化石油气时,在换气时要称量残气的质量予以补偿的原因是:丁烷的沸点高,在寒冷的冬天难以汽化,所以有较多的残气存在;由液化石油气的燃烧特点可知,消耗的氧气的量大,调整灶具的具体措施是:将进气口增大.
故答为:(1)天然气; 增大;有毒的CO生成,甚至有固体残留物堵塞燃气管道;(2)丁烷的沸点高,在寒冷的冬天难以汽化,所以有较多的残气存在;将进气口增大.
点评 本题考查甲烷、液化石油气的燃烧特点,解题的关键是根据基础知识和提供的信息联合解题,培养学生分析数据解题的能力.

练习册系列答案
相关题目
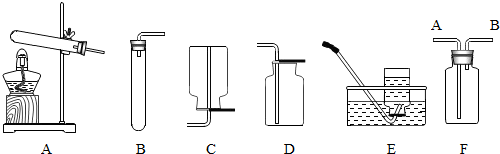
18.如图是实验室常用的气体制备、收集的多种功能装置.
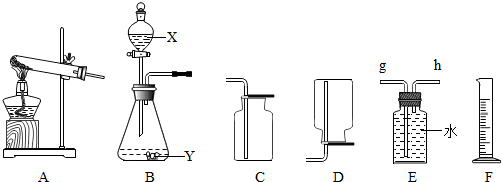
①若实验室用A装置加热氯酸钾和二氧化锰混合物制取氧气,其化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
②B装置中X装置的名称为分液漏斗;若B装置X中盛放稀盐酸、Y中盛放石灰石,B与C组成发生、收集CO2气体的系列装置,检验CO2收满的方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.检验制得气体是否为二氧化碳的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
③若实验室用锌粒和稀硫酸制取氢气,可选择的发生装置为B,发生的化学方程式为Zn+H2SO4=ZnSO4+H2↑.若用排水法收集并测定氢气的体积,氢气从E装置导管口h(填“g”或“h”)进.选用仪器F测量排出水的体积,仪器F的名称是量筒.
④对锌与稀硫酸反应快慢的影响因素进行探究.反应过程中,利用前10min内收集的氢气体积比较反应的快慢,控制其他条件相同,进行如图四组实验,获得数据如表:
要比较不同溶质质量分数的硫酸对反应快慢的影响,应选择的实验编号是a和c;可以得出的结论是:在其它条件相同的情况下,稀硫酸的溶质质量分数越大,反应速度越快.

①若实验室用A装置加热氯酸钾和二氧化锰混合物制取氧气,其化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
②B装置中X装置的名称为分液漏斗;若B装置X中盛放稀盐酸、Y中盛放石灰石,B与C组成发生、收集CO2气体的系列装置,检验CO2收满的方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.检验制得气体是否为二氧化碳的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
③若实验室用锌粒和稀硫酸制取氢气,可选择的发生装置为B,发生的化学方程式为Zn+H2SO4=ZnSO4+H2↑.若用排水法收集并测定氢气的体积,氢气从E装置导管口h(填“g”或“h”)进.选用仪器F测量排出水的体积,仪器F的名称是量筒.
④对锌与稀硫酸反应快慢的影响因素进行探究.反应过程中,利用前10min内收集的氢气体积比较反应的快慢,控制其他条件相同,进行如图四组实验,获得数据如表:
| 实验编号 | 试剂 | 前10min内产生的氢气体积/(mL) | |
| 不同纯度的锌 | 不同体积和溶质质量分数的稀硫酸 | ||
| a | 纯锌 | 30mL30% | 564.3 |
| b | 含杂质的锌 | 30mL30% | 634.7 |
| c | 纯锌 | 30mL20% | 449.3 |
| d | 纯锌 | 40mL30% | 602.8 |
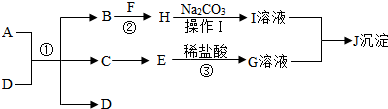 下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,如图是它们之间的转化关系,请回答:
下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,如图是它们之间的转化关系,请回答: