题目内容
4.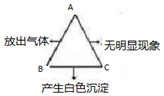 如图所示的A、B、C三种溶液两两混合,发生了化学反应同时产生的实验现象,其中A是初中化学常见的酸,请写出符合实验现象的一组物质的化学式和一个化学方程式.
如图所示的A、B、C三种溶液两两混合,发生了化学反应同时产生的实验现象,其中A是初中化学常见的酸,请写出符合实验现象的一组物质的化学式和一个化学方程式.(1)A:盐酸
(2)B:碳酸钠
(3)C:氢氧化钡
(4)化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑;Na2CO3+Ba(OH)2=BaCO3↓+2NaOH;Ba(OH)2+2HCl═BaCl2+2H2O.
分析 根据A、B、C三种溶液的现象可知,三种物质发生的是复分解反应,A是酸,A和C反应无现象,假设A是盐酸,B是可溶性碳酸盐,C是氢氧化钡或者可溶性钡盐,将三种物质的反应现象验证即可,
解答 解:
A、B、C三种溶液的现象可知,三种物质发生的是复分解反应,A是酸,A和C反应无现象,所以C是碱,B就是盐,假设A是盐酸,B是可溶性碳酸盐,C是氢氧化钡或者可溶性钡盐,盐酸和碳酸盐反应生成二氧化碳气体,盐酸和氢氧化钡或者钡盐发生反应无明显现象,碳酸盐和氢氧化钡或者可溶性钡盐反应生成白色的碳酸钡沉淀,满足题中的现象.
碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
碳酸钠和氢氧化钡反应生成碳酸钡和氢氧化钠,化学方程式为:Na2CO3+Ba(OH)2=BaCO3↓+2NaOH;
氢氧化钡和盐酸反应生成氯化钡和水,化学方程式为:Ba(OH)2+2HCl═BaCl2+2H2O.
故答案为:
盐酸、碳酸钠(碳酸钾等可溶性碳酸盐均可,但是当C为碱时就不能为碳酸铵)、氢氧化钡(或者可溶性的硝酸钡、氯化钡等,但是B为碳酸铵时本空不能是氢氧化钡).Na2CO3+2HCl═2NaCl+H2O+CO2↑;Na2CO3+Ba(OH)2=BaCO3↓+2NaOH;Ba(OH)2+2HCl═BaCl2+2H2O.
点评 在解此类题时,首先根据题中的现象分析物质的大致类别,然后进行猜想,最后验证猜想的正确性.

练习册系列答案
相关题目
15.推理是科学课学习中常用的思维方法.下列推理中正确的是( )
| A. | 碱溶液能使石蕊试液变蓝色,所以能使石蕊试液变蓝色的溶液一定是碱溶液 | |
| B. | 酸和碱反应生成盐和水,所以生成盐和水的反应一定是酸和碱的反应 | |
| C. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质不一定是碳酸盐 | |
| D. | 盐是由金属离子和酸根离子组成的,NH4NO3中没有金属离子,所以它不属于盐 |
19.下列有关金属及合金的说法中正确的是( )
| A. | 合金是由两种或两种以上金属熔合而成的具有金属特性的物质 | |
| B. | 在日常生活中,大量使用的常常不是纯金属,而是它们的合金 | |
| C. | “真金不怕火炼”说明黄金的硬度非常大 | |
| D. | 合金的熔点一般比它的成分金属熔点高 |
9.某学生为了验证铁、锌、铜三种金属的活动性顺序,设计了四种方案
①将Zn、Cu分别加入到FeSO4溶液中; ②将Zn、Cu分别加入到ZnSO4溶液中;
③将Zn分别加入到H2SO4、CuSO4溶液中; ④将Fe 分别加入到ZnSO4、CuSO4溶液中.
其中可行的是( )
①将Zn、Cu分别加入到FeSO4溶液中; ②将Zn、Cu分别加入到ZnSO4溶液中;
③将Zn分别加入到H2SO4、CuSO4溶液中; ④将Fe 分别加入到ZnSO4、CuSO4溶液中.
其中可行的是( )
| A. | ①④ | B. | ①② | C. | ②③ | D. | ③④ |
16.农夫山泉的传统产品主要为瓶装矿泉水,取自千岛湖的深层水.判断“农夫山泉”属于溶液的依据是( )
①无色②混合物③纯净物④均一性⑤稳定性.
①无色②混合物③纯净物④均一性⑤稳定性.
| A. | ①②④ | B. | ②④⑤ | C. | ①③⑤ | D. | ③④⑤ |
13.据《第一财经日报》报道,由于在本国遭禁,日韩聚氯乙烯(PVC)保鲜膜正转到中国销售,作为半成品包装.国家级权威机构专家介绍,PVC保鲜膜含有致癌物质,对人体危害较大.目前 LG、三菱、三荣三大品牌占中国市场近 80%的份额.聚氯乙烯(PVC)是由结构单元氯乙 烯(CH2CHCl)重复连接而成,其分子式为(CH2CHCl )n,下列说法错误的是( )
| A. | 不宜用 PVC 保鲜膜来包装熟食 | B. | PVC 是由三种元素组成 | ||
| C. | PVC 属于有机合成材料 | D. | PVC 的相对分子量是 62.5 |
2.我国化工专家侯德榜的“侯氏制碱法”为世界制碱 工业做出了突出的贡献.他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱.下表是几种物质在不同温度时的溶解度:
(1)从表中数据可以看出,温度对NaCl的溶解度影响不大.
(2)要使NH4C1饱和溶液中的NH4C1结晶析出,在较低(填“较高”或“较低”)温度下进行比较合适.
(3)“侯氏制碱法”制NaHCO3的方程式是NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl,进而生产出纯碱属于盐(填酸、碱、盐),它的浓溶液与澄清石灰水反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(1)从表中数据可以看出,温度对NaCl的溶解度影响不大.
(2)要使NH4C1饱和溶液中的NH4C1结晶析出,在较低(填“较高”或“较低”)温度下进行比较合适.
(3)“侯氏制碱法”制NaHCO3的方程式是NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl,进而生产出纯碱属于盐(填酸、碱、盐),它的浓溶液与澄清石灰水反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
| 0℃ | 20℃ | 40℃ | 60℃ | |
| NaHCO3 | 6.9 | 9.6 | 12.7 | 16.4 |
| NaCl | 35.7 | 35.8 | 36.6 | 37.3 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 |
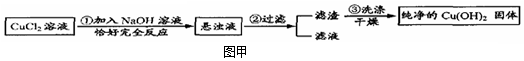
 将等质量的a、b两种金属粉末分别加入到等质量、等质量分数且足量的稀硫酸中,产生氢气的质量与实践的关系如图所示.请回答下列问题:(已知a、b两种金属元素在化合物中均为+2价)
将等质量的a、b两种金属粉末分别加入到等质量、等质量分数且足量的稀硫酸中,产生氢气的质量与实践的关系如图所示.请回答下列问题:(已知a、b两种金属元素在化合物中均为+2价) .
.