题目内容
11.化学-----我们的生活,我们的未来①化学使天更蓝,水更清.汽车尾气处理装置能使某些有毒气体转化为无毒气体:2NO+2CO→N2+2CO2,该反应涉及的物质中,N2在空气中含量最高;CO2是光合作用的原料;煤气中能与血红蛋白结合的有毒气体是CO;竹子可加工成具有吸附作用的物质,其作用与实验室中常用的活性炭(填物质名称)相似.
②化学为人类提供动力,氢能属于绿色能源,氢气燃烧的化学方程式是2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,可燃冰是一种新型能源,在我国南海储量很高,其主要成分为甲烷,甲烷的化学式为CH4.
分析 (1)根据空气中成分的体积含量考虑;根据物质的性质分析解答:二氧化碳是植物光合作用的原料,一氧化碳能与血红蛋白结合;
(2)根据氢气燃烧生成水分析;可燃冰是一种新型能源,在我国南海储量很高.其主要成分为甲烷.
解答 解:(1)空气中各成分及体积分数为:氮气:78%、氧气:21%、稀有气体:0.94%、二氧化碳0.03%、水蒸气和杂质:0.03%.所以氮气最多;光合作用的原料有二氧化碳和水,所给方程式中只能是二氧化碳;一氧化碳能与血红蛋白结合,使人体缺氧而中毒;具有吸附作用的物质有活性炭;故答案为:N2;CO2;CO;活性炭;
②氢气和氧气在点燃的条件下生成水,化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;可燃冰是一种新型能源,在我国南海储量很高.其主要成分为甲烷,其化学式为CH4,故答案为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;CH4;
点评 解答本题的关键是要知道空气中成分及其含量,光合作用的原料,及物质的性质,属于基础知识考查题.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
2.硅钢是变压器、充电器中的核心材料,其主要成份是Fe和Si.某学生用硅钢样品做了如下实验:取5.0g硅钢样品,将60g稀硫酸分6次加入样品中(其中稀硫酸与硅及其它杂质不反应),充分反应后过滤、洗涤、干燥、称重,得到的实验数据如表:
(1)表格中M=3.4.
(2)硅钢样品中铁的质量分数是84%.
(3)计算所用稀硫酸中溶质的质量分数.
| 实验次数 | 一 | 二 | 三 | 四 | 五 | 六 |
| 稀硫酸的用量/g | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 4.2 | M | 2.6 | 1.8 | 1.0 | 0.8 |
(2)硅钢样品中铁的质量分数是84%.
(3)计算所用稀硫酸中溶质的质量分数.
19.近几年饮食安全成为大家非常关心的话题,根据你学过的化学知识,下列做法正确的是( )
| A. | 食品中大量加入工业用盐亚硝酸钠 | |
| B. | 摄入过量含钙的营养补剂以防止骨质疏松 | |
| C. | 使用铁锅烹饪补充人体所需要的铁元素 | |
| D. | 蒸包子时在面粉中加入含铝添加剂 |
16.地壳中含量最多的元素是( )
| A. | 硅 | B. | 氧 | C. | 铝 | D. | 铁 |
20.某同学利用如图装置验证二氧化碳的相关化学性质.
(1)步骤①中发生反应的化学方程式是Ca(OH)2+CO2=CaCO3↓+H2O.
(2)补全步骤②中的现象:紫色石蕊溶液变红.
(3)补全步骤③中的现象:溶液由红色变为蓝色,其中“气球1继续变大”的原因是二氧化碳与氢氧化钠反应使容器内气体减少,压强减小.
(4)通过本实验能验证的二氧化碳的化学性质是二氧化碳分别能与水、氢氧化钙、氢氧化钠反应.
| 实验装置 | 实验步骤 | 实验现象 |
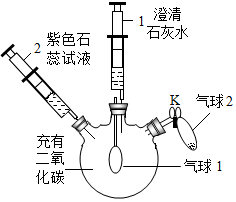 | ①向外拉注射器1 | 气球1微微鼓起, 注射器1中溶液变浑浊 |
| ②将注射器2中的液体推入瓶中 | 气球1继续微微鼓起, … | |
| ③打开K,将气球2中的固体氢氧化钠倒入瓶中后,关闭K | 气球1继续变大, … |
(2)补全步骤②中的现象:紫色石蕊溶液变红.
(3)补全步骤③中的现象:溶液由红色变为蓝色,其中“气球1继续变大”的原因是二氧化碳与氢氧化钠反应使容器内气体减少,压强减小.
(4)通过本实验能验证的二氧化碳的化学性质是二氧化碳分别能与水、氢氧化钙、氢氧化钠反应.
1.下列各组固体物质不能用水鉴别的是( )
| A. | NaOH和NH4NO3 | B. | CuSO4和Na2CO3 | C. | CaO和Ca(OH)2 | D. | Mg(OH)2和CaCO3 |