题目内容
10.硫酸亚铁在工农业生产中有重要用途,也有较高的医用价值.工业上用废铁屑和含硫酸的废液来制取硫酸亚铁,变废为宝.现用5.6t铁屑与100t废液恰好完全反应(已知铁屑只和废液中的硫酸反应),请你计算:(1)可生成硫酸亚铁的质量;
(2)所用废液中硫酸的溶质质量分数.
分析 铁和稀硫酸反应生成硫酸亚铁和氢气,关键反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)设硫酸的质量为x,可生成硫酸亚铁的质量为y,
Fe+H2SO4═FeSO4+H2↑,
56 98 152
5.6t x y
$\frac{56}{5.6t}$=$\frac{98}{x}$=$\frac{152}{y}$,
x=9.8t,y=15.2t,
答:可生成硫酸亚铁的质量是15.2t.
(2)所用废液中硫酸的溶质质量分数为:$\frac{9.8t}{100t}$×100%=9.8%,
答:所用废液中硫酸的溶质质量分数是9.8%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
1.下列说法错误的是( )
| A. | 干冰不是冰 | B. | 金刚石不是金 | C. | 纯碱不是碱 | D. | 食盐不是盐 |
5.下列四个实验方案设计不合理的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别氯化铵和尿素 | 分别加入熟石灰粉末研磨,闻气味 |
| B | 鉴别硝酸铵和氯化钠 | 分别加适量水,用手触摸容器壁 |
| C | 鉴别硫酸铜溶液和稀盐酸 | 分别观察溶液颜色 |
| D | 鉴别烧碱溶液和石灰水 | 分别滴加酚酞试液,观察颜色变化 |
| A. | A | B. | B | C. | C | D. | D |
15.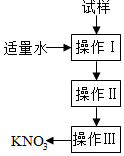 实验室有一包含有少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾,设计了如图所示的操作,下列有关分析中正确的是( )
实验室有一包含有少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾,设计了如图所示的操作,下列有关分析中正确的是( )
 实验室有一包含有少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾,设计了如图所示的操作,下列有关分析中正确的是( )
实验室有一包含有少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾,设计了如图所示的操作,下列有关分析中正确的是( )| A. | 操作Ⅰ~Ⅲ分别是溶解、加热蒸发、过滤 | |
| B. | 操作Ⅰ是过滤,将氯化钠固体从溶液中分离除去 | |
| C. | 操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠 | |
| D. | 操作Ⅲ是过滤,将硝酸钾晶体从溶液中分离出来 |
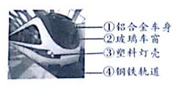 安徽合肥地铁1号线12月26日正式开通运营,这也标志着.合肥市民将迎来“地铁生活”,改变出现方式.如图是合肥地铁图:
安徽合肥地铁1号线12月26日正式开通运营,这也标志着.合肥市民将迎来“地铁生活”,改变出现方式.如图是合肥地铁图: