题目内容
7.下列生活用品不属于有机合成材料的是( )| A. | 塑料瓶 | B. | 不锈钢刀 | C. | 涤纶布料 | D. | 汽车轮胎 |
分析 有机合成材料简称合成材料,要判断是否属于合成材料,可抓住三个特征:有机物、合成、高分子化合物,据此常见材料的分类进行分析判断.
解答 解:A、塑料属于有机合成材料;
B、不锈钢属于金属材料;
C、涤纶属于有机合成材料;
D、汽车轮胎是橡胶制成的,属于有机合成材料;
故选B.
点评 本题难度不大,掌握合成材料的三大特征(有机物、合成、高分子化合物)、分类是正确解答此类题的关键所在.

练习册系列答案
相关题目
17.下列4个图象能正确反映对应变化关系是( )
| A | B | C | D |
 |  |  |  |
| 向一定量的氢氧化钠溶液中滴加稀盐酸 | 木炭在盛有氧气的密闭容器内燃烧 | 将水通电电解一段时间 | 室温下,向不饱和硝酸钾溶液中加入硝酸钾 |
| A. | A | B. | B | C. | C | D. | D |
15.某化学课外活动小组的同学在学习《化学》下册77页的资料卡片“石笋和钟乳石的形成”时,发现难溶于水的CaCO3当遇到溶有CO2的水时,会反应生成溶解性较大的Ca(HCO3)2:【CaCO3+CO2+H2O═Ca(HCO3)2】.联想到实验室检验CO2时,将气体通入澄清石灰水中.若长时间往澄清石灰水中通入CO2会产生什么样的现象呢?小组决定用小烧杯盛装一定量的氢氧化钠溶液并不断通入二氧化碳气体进行探究
【提出问题】氢氧化钠溶液中通入二氧化碳一段时间后,溶液中含有什么溶质?
【查阅资料】
(1)通入少量的二氧化碳时,NaOH与CO2反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O.
(2)通入过量CO2时,反应的化学方程式为:Na2CO3+CO2+H2O═2NaHCO3.
(3)碳酸氢盐都是可溶于水的.BaCO3难溶于水且是白色固体.
(4)Na2CO3、NaHCO3溶液呈碱性,BaCl2显中性.
【提出猜想】
(1)溶质为NaOH和Na2CO3;
(2)溶质为Na2CO3;
(3)溶质是NaHCO3、Na2CO3(填化学式);
(4)溶质全都是NaHCO3.
【设计实验方案】
【得出结论】猜想(3)成立.
【讨论交流】
(1)有同学提出实验步骤①是多余的.你认为该实验设计是否需要?并说明理由不需要,因为氢氧化钠、碳酸钠、碳酸氢钠溶液都为碱性.
(2)将实验步骤②剩下混合物进行过滤(填操作名称)、洗涤、干燥、称量,发现所得沉淀质量等于步骤②中所称量的溶液质量的十分之一,判断氢氧化钠溶液中通入二氧化碳一段时间后,溶液中 Na2CO3的质量分数约为B.
A.4.26% B.5.38% C.3.43%.10%
【反思应用】
验证二氧化碳性质时,如果长时间向澄清石灰水中通入二氧化碳会看到什么样的现象呢?请你描述一下石灰水先变浑浊,后又变回澄清.
【提出问题】氢氧化钠溶液中通入二氧化碳一段时间后,溶液中含有什么溶质?
【查阅资料】
(1)通入少量的二氧化碳时,NaOH与CO2反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O.
(2)通入过量CO2时,反应的化学方程式为:Na2CO3+CO2+H2O═2NaHCO3.
(3)碳酸氢盐都是可溶于水的.BaCO3难溶于水且是白色固体.
(4)Na2CO3、NaHCO3溶液呈碱性,BaCl2显中性.
【提出猜想】
(1)溶质为NaOH和Na2CO3;
(2)溶质为Na2CO3;
(3)溶质是NaHCO3、Na2CO3(填化学式);
(4)溶质全都是NaHCO3.
【设计实验方案】
| 实验步骤 | 实验现象 | 实验结论 |
| ①用试管取少量小烧杯中反应后的溶液,滴加几滴酚酞试液(填酸碱指示剂) | 溶液变红色 | 该溶液显碱性 |
| ②将小烧杯中反应后剩下的溶液进行称量,然后滴加过量的BaCl2溶液 | 有 白色沉淀生成 | 猜想(4)不成立 |
| ③取步骤②中的上层清液,滴入稀盐酸 | 有气泡冒出 | 猜想(1)和(2)不成立 |
【讨论交流】
(1)有同学提出实验步骤①是多余的.你认为该实验设计是否需要?并说明理由不需要,因为氢氧化钠、碳酸钠、碳酸氢钠溶液都为碱性.
(2)将实验步骤②剩下混合物进行过滤(填操作名称)、洗涤、干燥、称量,发现所得沉淀质量等于步骤②中所称量的溶液质量的十分之一,判断氢氧化钠溶液中通入二氧化碳一段时间后,溶液中 Na2CO3的质量分数约为B.
A.4.26% B.5.38% C.3.43%.10%
【反思应用】
验证二氧化碳性质时,如果长时间向澄清石灰水中通入二氧化碳会看到什么样的现象呢?请你描述一下石灰水先变浑浊,后又变回澄清.
2.下列过程中,只发生了物理变化的是( )
| A. | 铜器生锈 | B. | 粮食酿酒 | C. | 食物腐败 | D. | 冰雪融化 |
12.工业铁红主要成分是Fe2O3,还含有少量的FeO、Fe2O4.
【查阅资料】1.草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O4•3H2O$\frac{\underline{\;H_{2}SO_{4}\;}}{△}$CO2↑+CO↑+4H2O.
2.碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳.
3.铁的常见氧化物中铁的质量分数:
【问题讨论】为了测定铁红中铁的质量分数,小组同学进行如下实验.(装置气密性良好)
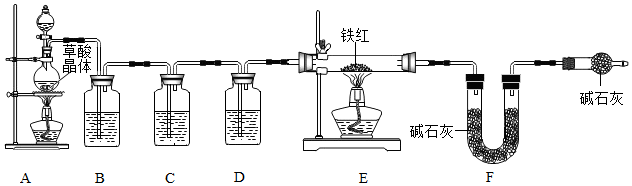
(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是cba.(填字母序号)
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(2)C装置的作用是检验二氧化碳是否除尽.
(3)写出E装置中所发生反应的一个化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(或4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2或CO+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2).
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①若E中充分反应后得到铁粉的质量为mg,则7.0<m<7.78.
②若实验前后称得F装置增重7.7g,则此铁红中铁的质量分数是72%.
【实验反思】
(1)如果缺少装置G(不考虑其他因素),则测得样品中铁的质量分数会偏小(选填“偏小”“不变”或“偏大”).
(2)该实验装置的一个明显缺陷是缺少尾气处理装置.
【查阅资料】1.草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O4•3H2O$\frac{\underline{\;H_{2}SO_{4}\;}}{△}$CO2↑+CO↑+4H2O.
2.碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳.
3.铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |

(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是cba.(填字母序号)
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(2)C装置的作用是检验二氧化碳是否除尽.
(3)写出E装置中所发生反应的一个化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(或4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2或CO+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2).
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①若E中充分反应后得到铁粉的质量为mg,则7.0<m<7.78.
②若实验前后称得F装置增重7.7g,则此铁红中铁的质量分数是72%.
【实验反思】
(1)如果缺少装置G(不考虑其他因素),则测得样品中铁的质量分数会偏小(选填“偏小”“不变”或“偏大”).
(2)该实验装置的一个明显缺陷是缺少尾气处理装置.

 实验室中有一瓶酸溶液X,已知是稀盐酸和稀硫酸中的一种,另有一固体混合物A,其中可能含有Mg、NH4Cl、NaCl、K2SO4中的两种或多种,按如图所示进行探究实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应).
实验室中有一瓶酸溶液X,已知是稀盐酸和稀硫酸中的一种,另有一固体混合物A,其中可能含有Mg、NH4Cl、NaCl、K2SO4中的两种或多种,按如图所示进行探究实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应).