题目内容
18.碳酸钠和氯化钡溶液反应,不仅可以用Na2CO3+BaCl2=BaCO3↓+2NaCl表示,还可以用CO32-+Ba2+=BaCO3↓表示,后者叫离子方程式.书写离子方程式的步骤如下:①“写”:写出化学方程式.(Na2CO3+BaCl2=BaCO3↓+2NaCl)
②“拆”:将易溶易电离的酸、碱和盐拆写成离子形式;沉淀、气体和水仍用化学式表示,不能拆写成离子形式.(2Na++CO32-+Ba2++2C1-=BaCO3↓+2Na++2C1-)
③“删”:删去方程式左右两边相同的离子.(CO32-+Ba2+=BaCO3↓)
④“查”:检查方程式左右两边各元素的原子个数和电荷总数是否相等.
注意:离子方程式中生成物为沉淀或气体时需标出“↓”或“↑”.
根据以上信息,结合已学知识,回答下列问题:
(1)NaOH在水中电离出OH-(填阴离子符号);
(2)Na2CO3+H2SO4=Na2SO4+CO2↑+H2O的离子方程式是CO32-+2H+=CO2↑+H2O.
分析 根据氢氧化钠中的阴离子是氢氧根离子,结合化学反应的实质书写离子反应方程式.
解答 解:(1)氢氧化钠在水中电离出的阴离子是氢氧根离子,故填:OH-;
(2)Na2CO3+H2SO4=Na2SO4+CO2↑+H2O反应的实质是碳酸根离子与氢离子反应生成水和二氧化碳,故填:CO32-+2H+=CO2↑+H2O.
点评 掌握化学的实质是正确解答本题的关键.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
8.固体碘受热升华,下列关于此过程的说法正确的是( )
| A. | 碘分子体积变大 | B. | 碘分子运动速率不变 | ||
| C. | 碘分子质量变大 | D. | 碘分子间的间隔变大 |
7.下列生活用品不属于有机合成材料的是( )
| A. | 塑料瓶 | B. | 不锈钢刀 | C. | 涤纶布料 | D. | 汽车轮胎 |
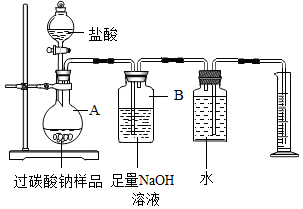 “氧泡泡”系列产品去污能力强、绿色环保,已成为中国氧系清洁品类领导品牌,其主要成分是过碳酸钠(2Na2CO3•3H2O2).某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究.
“氧泡泡”系列产品去污能力强、绿色环保,已成为中国氧系清洁品类领导品牌,其主要成分是过碳酸钠(2Na2CO3•3H2O2).某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究.