题目内容
19.下列图象与对应选项关系不合理的是( )| A. | 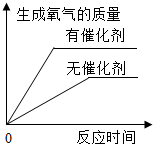 用相等质量的双氧水来制取氧气 | |
| B. | 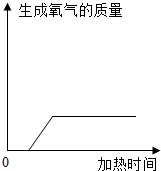 加热氯酸钾与二氧化锰的混合物制氧气 | |
| C. | 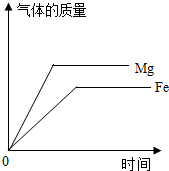 等质量的镁和铁分别与足量的同一浓度稀硫酸反应 | |
| D. | 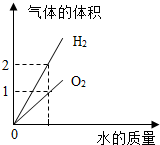 电解水生成氧气和氢气 |
分析 A、根据催化剂只会影响反应速率,不会影响生成氧气的量进行分析;
B、根据加热氯酸钾制取氧气时,需要加热一段时间才能分解生成氧气进行分析;
C、根据镁、铁的相对原子质量和金属活动性顺序进行分析;
D、根据通电分解水的实验现象及结论进行分析.
解答 解:A、过氧化氢分解的过程中催化剂,只能加快过氧化氢溶液的分解速率而生成氧气的质量在反应前后不会改变,故A错误;
B、加热氯酸钾制取氧气时,需要加热一段时间才能分解生成氧气,故B正确;
C、镁比铁活泼,镁的相对原子质量比铁小,所以镁比铁反应快,生成的氢气多,故C正确;
D、通电分解水时产生氢气的体积是氧气的二倍,不是质量比,故D正确.
故选:A.
点评 根据所给的问题情景及相关信息,结合所学的相关知识和技能,联系起来细心地探究、推理后,按照题目要求进行选择或解答即可.

练习册系列答案
相关题目
9.下列说法正确的是( )
| A. | 分子是化学变化中的最小粒子 | B. | 有单质生成的反应都是置换反应 | ||
| C. | 氧化物是含氧元素的化合物 | D. | 木炭和活性炭都具有吸附作用 |
10.下列物质的性质与用途没有直接关系的是( )
| A. | 铜能导电--用作电线 | |
| B. | 稀有气体化学性质稳定--用作保护气 | |
| C. | 氧气密度比空气略大--用于急救病人 | |
| D. | 氢氧化钙可用来改良酸性土壤--溶液呈碱性 |
7.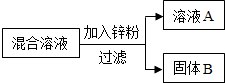 某化学实验小组用一定量AgNO3和 Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分进行了分析和实验研究.
某化学实验小组用一定量AgNO3和 Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分进行了分析和实验研究.
【提出问题】溶液A中的溶质可能由哪些?
【作出猜想】猜想①只有Zn(NO3)2;
猜想②Zn(NO3)2、AgNO3;
猜想③Zn(NO3)2、Cu(NO3)2;
猜想④Zn(NO3)2、AgNO3、Cu(NO3)2.
【讨论交流】
若猜想③成立,则溶液A呈蓝色,固体B中一定不含的金属Zn(写化学式).四种猜想中不合理的猜想是②(填标号),其理由是猜想②中无硝酸铜,说明Cu(NO3)2已与锌反应生成Cu,而铜能与硝酸银反应,所以不可能存在硝酸银.
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请填写下表.
 某化学实验小组用一定量AgNO3和 Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分进行了分析和实验研究.
某化学实验小组用一定量AgNO3和 Cu(NO3)2混合溶液进行了如图实验,并对溶液A和固体B的成分进行了分析和实验研究.【提出问题】溶液A中的溶质可能由哪些?
【作出猜想】猜想①只有Zn(NO3)2;
猜想②Zn(NO3)2、AgNO3;
猜想③Zn(NO3)2、Cu(NO3)2;
猜想④Zn(NO3)2、AgNO3、Cu(NO3)2.
【讨论交流】
若猜想③成立,则溶液A呈蓝色,固体B中一定不含的金属Zn(写化学式).四种猜想中不合理的猜想是②(填标号),其理由是猜想②中无硝酸铜,说明Cu(NO3)2已与锌反应生成Cu,而铜能与硝酸银反应,所以不可能存在硝酸银.
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请填写下表.
| 实验步骤 | 现象 | 固体B的组成(写化学式) |
| 取少量固体B,滴加 稀盐酸 | 有气泡产生 | Zn、Cu、Ag |
14.2016年8月5日-8月21日奥运会将在巴西里约热内卢进行.下列运动设施中没有用到合成有机高分子材料的是( )
| A. | 跑步、跳远使用的塑胶跑道 | B. | 排球、羽毛球使用的化纤网 | ||
| C. | 单杠、双杠使用的钢制或木质横梁 | D. | 跳高、拳击使用的海绵护垫 |
11.2014年5月上旬,一枚用于探伤的放射源铱192(铱原子中含有77个质子和115个中子)在南京丢失,引起了社会的广泛关注.下列说法正确的是( )
| A. | 该元素属于金属元素 | B. | 该元素的原子序数是192 | ||
| C. | 该原子的核外有115个电子 | D. | 该原子的相对原子质量192g |
8.小刚同学在实验室中用过氧化氢制取了氧气,实验又展开了下列思考与探究:
【问题一】:催化剂MnO2的用量对反应速率有没有影响呢?
设计实验:每次均用同体积同浓度的H2O2溶液,采用不同量MnO2粉末做催化剂来反应,测定各次收集相同体积氧气时所用的时间.
小刚进行实验后(其它实验条件均相同,所得数据如下:
由表中数据可以得到相应的结论是二氧化锰的量会影响过氧化氢的反应速率,且在一定范围内,二氧化锰的量越大,反应速率越快.
【问题二】H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取同体积不同浓度的H2O2溶液进行实验,记录数据如下:(实验均在20℃室温下进行,其它实验条件也均相同)
由表中数据可以得到的结论是过氧化氢溶液的溶质质量分数越大,化学反应速率越快.
【问题三】还有那些因素可能影响该反应速率呢?请你说出一个猜想:温度.
可验证你猜想的实验方案为:分别取相同体积相同浓度的过氧化氢溶液、等量的二氧化锰粉末,在不同温度下反应,测定收集相同体积氧气时所用的时间..
【问题一】:催化剂MnO2的用量对反应速率有没有影响呢?
设计实验:每次均用同体积同浓度的H2O2溶液,采用不同量MnO2粉末做催化剂来反应,测定各次收集相同体积氧气时所用的时间.
小刚进行实验后(其它实验条件均相同,所得数据如下:
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间 | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
【问题二】H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取同体积不同浓度的H2O2溶液进行实验,记录数据如下:(实验均在20℃室温下进行,其它实验条件也均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| MnO2粉末用量/克 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集到540mL气体所用时间/秒 | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
【问题三】还有那些因素可能影响该反应速率呢?请你说出一个猜想:温度.
可验证你猜想的实验方案为:分别取相同体积相同浓度的过氧化氢溶液、等量的二氧化锰粉末,在不同温度下反应,测定收集相同体积氧气时所用的时间..